


Hola!
En la sesión de formación que sigue, encontrará todo lo que necesita saber acerca de la Física básica: pH. Al finalizar la sesión de formación hay un test de conocimientos, que le permitirá comprobar cuánto recuerda del tema.
Duración: aproximadamente 45 min.
Inicie el capítulo con la flecha de abajo a la derecha.
¡Que disfrute!
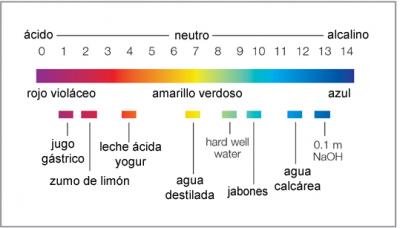
La abreviatura pH es la expresión latina "pondus Hydrogenii" y cuando se traduce tiene el significado base absoluta de hidrógeno.
Por lo tanto, el pH es una medida de la concentración de iones H3O+ (iones hidronio) en una sustancia.
Como resultado de esta concentración se pueden hacer conclusiones precisas del carácter ácido y neutro o alcalino (básico) de una sustancia.
El pH es un importante parámetro a medir en muchos procesos químicos y bioquímicos. Por ejemplo, el grado de madurez del queso y de la carne o el grado de acidez de la masa ácida y de los baños galvánicos.
El pH también juega un papel importante en las industrias farmacéuticas y medioambientales.
La escala de pH: Así pues, la escala de pH es una escala logarítmica decimal que va normalmente desde 0 (muy ácido) a 14 (muy alcalino). También se pueden encontrar pHs que son inferiores a 0 y superiores a 14 en ácidos o lejías con elevadas concentraciones. Si la sustancia tiene un pH 7, tiene un carácter neutro.
Cálculo del pH:
pH = -log [H+]
[H+] = Concentración de ión hidronio
Ejemplo:
Concentración de H+ = 10-4 mol/l es equivalente a un pH = 4
1 mol (cantidad de material) = 6.022x10^23 partículas

La medición del pH es la conversión de la concentración de iones hidronio en una tensión eléctrica. A finales del siglo XIX se realizaron experimentos utilizando placas de platino pulido y puentes de electrolito (soluciones salinas) para poder realizarlo.
Como el electrolito se consume y los valores medidos se deben referir a una referencia para obtener valores estables, se ha introducido el sistema de dos electrodos para esta finalidad.
En el electrodo de medición se genera un potencial que es proporcional a la concentración de iones de hidrógeno (pH). El electrodo de referencia proporciona la referencia de potencial del sistema. El pH se traduce en una diferencia de potencial o tensión eléctrica entre el electrodo de medición y el electrodo de referencia que puede ser interpretada por circuitos electrónicos para poder mostrar su valor. En el ámbito del progreso técnico, se ha ideado mejorar el complicado manejo de los dos sensores (uso de laboratorio) mediante la integración de ambos canales de medición en un electrodo individual, el llamado electrodo combinado.
Actualmente, se utilizan casi exclusivamente electrodos combinados de pH.
Electrodo de medición:
El electrodo de vidrio posee las mejores características técnicas de medición posibles de todos los sensores que existen.
Además de su manejo sencillo, también ofrece la mayor precisión posible. Se puede aplicar universalmente y es muy resistente a las influencias de la solución tales como color, viscosidad y composición química.
La pieza central de este electrodo de medición es una membrana de vidrio muy delgada (membrana de pH) fabricada con un vidrio selectivo del pH especial. Este vidrio tiene la capacidad de reaccionar con la humedad o el agua de forma que se crea una finísima capa invisible que contiene agua sobre la superficie. Este gel o capa se utiliza como barrera selectiva que, prácticamente, solo intercambia los iones H+ con la solución a medir. El intercambio de otros iones se bloquea.

El electrodo de referencia tiene la tarea de proporcionar un potencial de referencia constante.
Cada electrodo de referencia consta de un elemento de referencia que está colocado en una solución electrolítica definida. Este electrolito debe tener contacto con el medio a medir. En los electrodos de referencia corrientes la conexión se realiza usando el llamado diafragma que garantiza flujo de iones.
El diafragma:
Existen varios tipos de diafragmas: un pin de madera, una espiga cerámica porosa, un pequeño agujero, vidrio molido, un poro o un haz de fibras, sólo por nombrar unos pocos.
El tipo a utilizar depende de la tarea de medición, pero con mayor frecuencia, de la filosofía de la empresa fabricante del electrodo de que se trate. El más ampliamente usado diafragma cerámico puede dar lugar a problemas debido a su estructura porosa tipo esponja. Se obstruye y la lectura se hace inestable.
No obstante, el mayor número de tareas de medición que se realizan en el uso diario utilizan diafragmas cerámicos “sin mantenimiento”.
El potencial del sistema de referencia está definido por los electrolitos de referencia y el elemento de referencia.
Normalmente se utiliza como electrolito de referencia una solución 3 M de cloruro potásico (KCI). El elemento de referencia está compuesto, normalmente, por un hilo de plata clorado.
Por razones de compensación electroquímica, también se debe disolver cloruro de plata (AgCI) en los electrolitos de referencia. Como el AgCI puede dar lugar a obstrucciones en el diafragma (cerámico) con algunas soluciones de medición, se colocan en el sistema de referencia electrodos de pH más recientes con un llamado cartucho donde se retiene el AgCI. El electrolito de referencia usado para rellenar debe estar libre de AgCI.
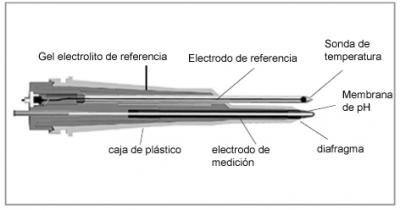
Los electrodos de medición y de referencia separados solamente son de utilidad cuando tienen grandes diferencias en su vida estimada. En la práctica, el electrodo combinado es el más utilizado en la actualidad. En comparación con la configuración separada, es más fácil de usar. El electrodo de medición y el electrodo de referencia se combinan en una sola unidad con el electrodo combinado.
Por lo tanto, junto con un sensor de temperatura integrado adicional, solamente se requiere una única sonda para medir el pH. Con este tipo de estructura de electrodo, existen soluciones de cloruro potásico (KCI) 3 M en forma líquida con el electrolito de referencia.
Este líquido se puede introducir a través de una abertura de relleno. Las sondas de este tipo tienen una duración muy grande. Sin embargo, tienen la desventaja de que la solución de electrolito de referencia se debe rellenar de forma regular.
Si este electrolito de referencia se sustituye por un gel, esto se conoce como un electrodo de gel.
La medida del pH con el llamado electrodo de vidrio de pH es el método más corriente utilizado en la actualidad.
Mediante este método, el electrodo de vidrio genera un voltaje proporcional al pH.
Como el electrodo solo puede generar una pequeña cantidad de tensión eléctrica (los profesionales hablan de una elevada resistencia eléctrica interna), se habla de medición potenciométrica con un sensor electroquímico.
Los sensores electroquímicos transmiten un voltaje que cambia con la concentración de iones hidronio del medio. Dependiendo del tipo de sensor y de la calidad de la calibración, se pueden conseguir exactitudes bastante superiores a ± 0,03 unidades de pH.
Los electrodos de vidrio de pH se caracterizan por su amplio rango de medición con elevadas precisiones y manejo sencillo y se pueden aplicar en muchas áreas ante todo. Otros ejemplos de electrodos son los electrodos de hidrógeno, de quinhidrona, de antimonio y de bismuto. Además, existen sensores de pH con tecnologías de semiconductores (ISFET’s), pero sus señales no las pueden evaluar los phmetros comunes.
Instrumentos de medición compactos:
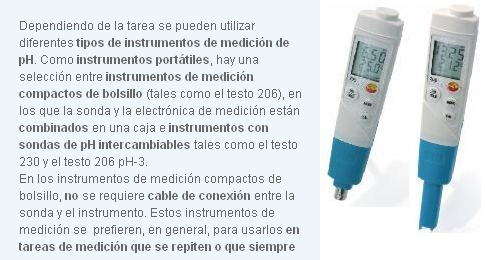
Sistemas de medición:

Los electrodos de pH Testo patentados son electrodos combinados con sonda de temperatura integrada. Esto también permite realizar una medición de la temperatura además de registrar el pH utilizando electrodos de penetración. Como electrolito se utiliza un gel de polímero.
Los electrodos tienen una mayor duración que los electrodos comparables como consecuencia del tamaño del espacio interior (volumen de relleno).

Hoja informativa:


La calibración es la determinación y documentación de una desviación. Se compara la lectura con un valor nominal y se establece la desviación. El instrumento de medición todavía presenta el valor "erróneo" pero se conoce su desviación del valor fijado. En este caso, el término calibración se utiliza como término que incluye la calibración y el ajuste.
El ajuste es la fijación del instrumento de medición a la desviación determinada durante la calibración.
¿Por qué se deben hacer calibraciones?
La estructura interna de un electrodo de pH ha sido diseñada para que genere una tensión eléctrica de 0 mV con una solución de medición de pH 7,00. Esta se llama el punto cero. El punto cero real se desvía un poco de éste. Por lo tanto, el electrodo suministra un voltaje que se desvia ligeramente (por ejemplo, +5 mV) a pH 7,00.
Una razón para ello es el envejecimiento de los electrodos de pH. Por lo tanto se realiza una compensación del punto cero para esta finalidad, durante la calibración.
El cambio de tensión por unidad de pH (mV/pH) se llama la pendiente. Ésta también depende del estado del electrodo de pH. Como el punto cero y su pendiente pueden cambiar por las condiciones de medición externas así como por el proceso natural de envejecimiento, un electrodo de pH se debe calibrar de forma regular.
¿Cómo se hace una calibración?
La tensión del punto cero (mV) así como la pendiente (mV/pH) de un electrodo de pH se determinan mediante la calibración y se guardan en el instrumento de medición. Sólo entonces cada tensión medida puede tener asignada un valor de pH. Para esta finalidad se debe sumergir una sonda en las soluciones buffer de pH respectivas.
Se debe tener en cuenta que la temperatura tiene influencia sobre el pH. Para esta finalidad es importante que se conozca y guarde en el instrumento la variación exacta de la temperatura de los buffer de pH utilizados. Además, la temperatura real se debe traspasar al instrumento de medición. Esto se puede efectuar automáticamente con una sonda de temperatura o manualmente realizando una introducción usando el teclado.
¿Cuándo se debe realizar la calibración?
La calibración se debe repetir tan pronto como la comprobación con un pH estándar muestre que la lectura indicada por el instrumento de medición no corresponde con el valor impreso en la solución buffer.
Se debe tener en cuenta la exactitud requerida obtenida en la medida.

Ahora acaba de finalizar el capítulo Diseño y funcionamiento.
¿Recuerda los conceptos más importantes? Intente responder para Ud. las siguientes preguntas, y recorra nuevamente el capítulo si tiene dudas...
Preguntas:
Un patrón es una norma elaborada por un organismo de normalización tal como el Instituto Alemán de Normas o la Organización Internacional para la Estandarización.

Antes de la puesta en servicio, en primer lugar se debe comprobar visualmente el estado sin problemas del instrumento de medición así como de los electrodos (nivel de líquido, vidrio roto, tapón de cierre).
Si es necesario se debe calibrar el sistema de medición con arreglo a las instrucciones del fabricante. Se debe hacer la comprobación de que el electrodo y el instrumento han sido seleccionados correctamente para la aplicación.

En primer lugar se conecta el electrodo al pHmetro (no aplica con electrodos fijos). Luego se debe lavar el electrodo con agua y se seca con una toalla, pero sin frotar. Frotar puede generar cargas eléctricas en la membrana de vidrio y provocará retardos en la visualización.
El proceso de medición:
Si el electrodo ha sido preparado, luego se sumerge en la solución a medir, se agita un poco y luego se deja reposar. Al hacerlo se debe sumergir el electrodo para que al menos un diafragma esté cubierto por la solución.
Se pueden observar diferentes valores de pH en soluciones agitadas y en reposo; normalmente, los valores de pH "imperturbables" son más exactos. Ello se debe a que la tensión generada en la solución durante la agitación influye sobre el resultado de la medición de forma negativa.
Tan pronto como se ha alcanzado una lectura estable (por ejemplo, con la ayuda de una función "Hold" automática), lea el valor, imprímalo y guarde o transmítalo directamente al ordenador. Entonces finaliza la medición.
Después de la medición aclare el electrodo con agua corriente y guárdelo con arreglo a las instrucciones del fabricante.
Error de medición:
Como ya se ha mencionado, muchos factores influyen sobre la medición del pH. Estos factores se originan químicamente (impurezas) o físicamente (influencias mecánicas tales como grietas en la membrana de vidrio) o son el resultado de errores de la medición y el envejecimiento del electrodo.
Las aplicaciones típicas para mediciones de pH se encuentran en muchos campos. A continuación se indican unas pocas de estas aplicaciones.
Aplicaciones: