


Hola!
en los próximos 90 minutos, más o menos, encontrará mucha información sobre el tema físico de "emisiones". Se describirán conceptos técnicos básicos, el diseño y el funcionamiento de los medidores de emisiones y las normas y aplicaciones correspondientes.
Inicie el capítulo con la flecha de abajo a la derecha.
¡Páselo bien!

La energía (del griego) significa "fuerza activa " y se define como la capacidad de una sustancia, cuerpo o sistema para realizar trabajo. La energía se puede manifestar en diferentes tipos de energía dependiendo de su forma. Sencillamente hay seis categorías:
Tipos de Energía:
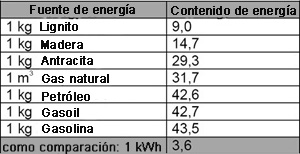
Los diversos tipos de energía se pueden convertir entre sí, aunque en un sistema cerrado ideal la suma de todas las energías permanecerá la misma (principio de conservación de la energía). Esto aplica realmente con relación al universo como sistema. Sin embargo, en la práctica, la energía se pierde en mayor o menor medida cuando se convierte y esta pérdida afecta al rendimiento del proceso de conversión. Las fuentes de energía que se encuentran en la naturaleza (carbón, gas natural, petróleo, luz solar, energía hidráulica) se denominan energías primarias, mientras que las formas de energía generadas convirtiendo estas energías primarias (electricidad, calor, etc.) se llaman energías secundarias. Las fuentes de energía mencionadas anteriormente no solo difieren en su forma sino, también, en su contenido de energía. Con fines de comparación, se especifica generalmente la cantidad de energía que se podría liberar si se quemara completamente una cantidad dada de una fuente de energía. La Tabla 1 proporciona unos pocos ejemplos ilustrativos. La unidad de medición de la energía es el Julio (J).
Contenido de energía de diversos combustibles:
Combustión:
La combustión es la conversión de la energía química primaria contenida en combustibles tales como carbón, petróleo y madera en energía calorífica secundaria por medio de un proceso de oxidación. La combustión es, por consiguiente, el término técnico para la reacción del oxígeno con los constituyentes inflamables de combustibles, que libera energía.
Las combustiones tienen lugar a temperaturas elevadas (hasta 1000°C y superiores) y desprenden calor. El oxígeno necesario se aporta como parte del aire de combustión. Al mismo tiempo, se genera un volumen significativo de gases de combustión y, dependiendo del tipo de combustible, determinada cantidad de residuos (cenizas, carbonilla).
Oxidación:
Denominación de todas las reacciones químicas en las que una sustancia se combina con el oxígeno. Las oxidaciones incluyen la disipación de energía y son muy importantes en la ingeniería (combustión) y la biología (respiración), por ejemplo.

Las instalaciones de combustión son instalaciones para generar calor quemando combustibles sólidos, líquidos o gaseosos. Se requieren en diversos campos, por ejemplo:
La combustión tiene lugar en una caldera; otras partes de la instalación suministran y distribuyen el combustible, suministran el aire de combustión, transmiten el calor y retiran los gases de combustión y los residuos de la combustión (cenizas y carbonilla).
Los gases de combustión:
Los gases de combustión de las instalaciones de combustión contienen los productos de la reacción entre el combustible y el aire de combustión así como los residuos; estos productos están constituidos, principalmente, por polvo, óxidos de azufre, óxidos de nitrógeno y monóxido de carbono. Si se quema carbón, los gases de combustión también pueden contener HCl y HF y si se queman residuos, los constituyentes de éstos (HCl y HF de nuevo, así como diversos hidrocarburos, metales pesados, etc.) se encontrarán en los gases de combustión.
Como parte de la reglamentación de protección medioambiental, los gases de combustión de las instalaciones de combustión están sujetos a una estricta reglamentación por lo que respecta a los límites permitidos de contaminantes tales como polvo, óxidos de azufre, óxidos de nitrógeno y monóxido de carbono en los gases limpios (a su liberación a la atmósfera). Para cumplir con estos valores límite, las instalaciones de combustión están provistas de grandes instalaciones para limpiar los gases de combustión, tales como filtros de polvo y diversos lavadores de gases de combustión.
En España, los requisitos específicos están estipulados en los Reales Decretos 833/1975, 653/2003 y 430/2004.
Combustibles:
Pueden existir en diversas formas y composiciones:
Composición del combustible:
El conocimiento de la composición del combustible es esencial para gestionar la combustión lo más eficiente, y por consiguiente, económicamente posible. Incrementar la proporción de sustancias no inflamables (inertes) reduce el poder calorífico bruto / neto y aumenta la suciedad de las superficies de calefacción. Un mayor contenido de agua sube el punto de rocío del vapor de agua y consume energía del combustible para evaporar el agua en los gases de combustión. El azufre contenido en el combustible se convierte en SO2 y SO3 durante la combustión, lo que puede producir ácido sulfuroso o ácido sulfúrico agresivos cuando el gas se enfría por debajo del punto de rocío.

El aire de combustión proporciona el oxígeno necesario para la combustión. Está compuesto por nitrógeno (N2), oxígeno (O2), bajos volúmenes de gases inertes y una parte variable de vapor de agua. En algunos casos, se utiliza para la combustión oxígeno puro o una mezcla de oxígeno y aire.Los principales constituyentes del aire de combustión (con la excepción del oxígeno, que se consume durante la combustión) se encuentran en los gases de combustión.
Combustión ideal, coeficiente de exceso de aire, balance de materiales:
Combustión ideal, coeficiente de exceso de aire, balance de materiales. La necesidad mínima de oxígeno para la combustión completa (ideal) de las partes inflamables depende de la composición del combustible.
1 kg de carbono, por ejemplo, necesita 2,67 kg de oxígeno para quemarse, mientras que 1 kg de hidrógeno necesita 8 kg y 1 kg de azufre sólo 1 kg de oxígeno. En este caso, la combustión cuando las proporciones de las cantidades son exactas se denomina como combustión ideal o combustión en condiciones estequiométricas.
Las ecuaciones de reacción correspondientes son como sigue:
Carbono: C + O2 ----> CO2
Hidrógeno: 2H2 + O2 ----> 2H2O
Azufre: S + O2 ----> SO2
Composición del aire puro y seco en la superficie terrestre:
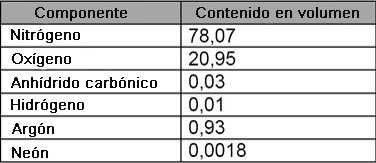
La combustión ideal se puede basar en el modelo mostrado en la Figura 1:
Modelo de una combustión ideal:
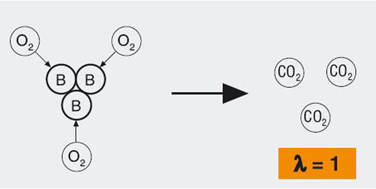
La cantidad de oxígeno suministrado es suficiente para quemar totalmente el combustible presente; no hay exceso de oxígeno ni de combustible.
En la práctica, sin embargo, esta cantidad ideal (mínima) de oxígeno no es suficiente para una combustión completa debido a la mezcla incompleta del combustible y el oxígeno, entre otras cosas, y se debe aportar más oxígeno y por consiguiente más aire de combustión de lo que es estequiométricamente necesario. Esta cantidad adicional de aire se conoce como "exceso de aire", la proporción entre la cantidad de aire real y la estequiométricamente necesaria se conoce como coeficiente de exceso de aire (Lambda). La Fig. 2 muestra esta situación en forma de modelo; debido al exceso de aire, aquí Lambda > 1.
Modelo de la combustión con exceso de aire:
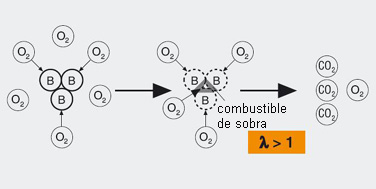

El rendimiento de la combustión máximo se consigue, por consiguiente, donde hay un exceso de aire u oxígeno mínimo, es decir, donde l > 1 (atmósfera oxidante).
Atmósfera oxidante:
Aquí hay mayor presencia de oxígeno de la que es necesaria para oxidar las sustancias oxidables en el combustible. Por consiguiente, es posible la oxidación (combustión) completa.
En términos sencillos: Oxidación = adición de oxígeno (el CO se oxida para formar CO2)
Atmósfera reductora:
En este caso hay muy poco oxígeno para oxidar todas las sustancias oxidables. Se produce lo contrario de una oxidación: una reducción.
En términos sencillos: Reducción = eliminación de oxígeno (el SO2 se reduce a S).
Determinación del coeficiente de exceso de aire:
El coeficiente de exceso de aire se puede determinar a partir de las concentraciones de los componentes de los gases de combustión CO, CO2 y O2; las correlaciones se muestran en lo que se denomina como el diagrama de combustión. Si el combustible y el aire se mezclan lo más perfectamente posible, hay un determinado contenido de CO (en el rango Lambda < 1) o un determinado contenido de O2 (en el rango Lambda > 1) para cada contenido de CO2. El valor de CO2 por sí solo no es claro debido a que el perfil de la curva va más allá del máximo, lo que significa que se requiere un ensayo adicional para establecer si el gas también contiene CO u O2 además del CO2. Para trabajar con exceso de aire (es decir, las condiciones normales), se prefiere ahora, en general, una medición de O2. Los perfiles de la curva son específicos del combustible, es decir, hay un diagrama individual y en particular un valor máximo específico de CO2 para cada combustible. Las relaciones entre estos numerosos diagramas se resumen frecuentemente en la práctica en forma de un ábaco ("triángulo de colores", no mostrado aquí).
Este se puede aplicar a cualquier tipo de combustible.
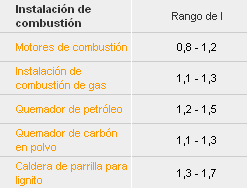
La tabla que sigue da los intervalos típicos del coeficiente de exceso de aire para determinadas instalaciones de combustión. En principio: cuanto menor es la superficie de reacción del combustible en relación con la unidad de masa (combustible de grano grueso), mayor es la cantidad de exceso de aire que se debe escoger para garantizar la combustión completa. Lo contrario también es cierto, y por esta razón los combustibles sólidos se muelen finamente y los combustibles líquidos se atomizan. Sin embargo, procesos especiales tales como el tratamiento térmico superficial se completan deliberadamente donde hay falta de aire, Lambda < 1, ya que esto es necesario para garantizar el proceso deseado.
Las dos fórmulas que siguen se aplican aproximadamente al cálculo teórico del coeficiente de exceso de aire a partir de las lecturas de CO2 o de O2:
Fórmulas para determinar el coeficiente de exceso de aire:
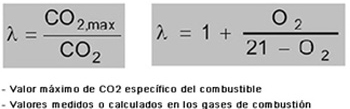
Rangos típicos del coeficiente de exceso de aire:

Las necesidades reales de aire se calculan:
Para el aire seco a la presión atmosférica este es 20,95%. En la práctica, sin embargo, el aire ambiente que se usa como aire de combustión nunca está totalmente seco, lo que significa que la humedad relativa también ha de tenerse en cuenta para el cálculo de la cantidad de aire, para garantizar un proceso exacto.
Volumen de gas, efecto de dilución, valor de referencia:
El aire de combustión y la humedad (vapor de agua) aumentan el volumen absoluto del gas. El gráfico que sigue ilustra este fenómeno para la combustión de 1 kg de combustible. En condiciones estequiométricas, es decir, sin exceso de aire, ésta produce aproximadamente 10 m3 de gases de combustión secos y 11,2 m3 húmedos, mientras que la misma cantidad de combustible, cuando se quema con un 25% de exceso de aire, produce un volumen de gases de combustión de 13,9 m3 húmedos. Esto tiene el mismo efecto que una dilución, ¡lo que reduce las proporciones relativas de los constituyentes de los gases de combustión! Por ejemplo, el contenido totalmente constante de SO2 baja en términos relativos desde un 0,2% (estequiométrico, seco) a un 0,18% (estequiométrico, húmedo) o 0,14% (25% de exceso de aire, húmedo), el contenido de oxígeno baja del 4,4% al 4%.
Véase también la tabla sobre el "Efecto sobre la combustión del contenido en humedad y el exceso de aire"
Composición relativa:
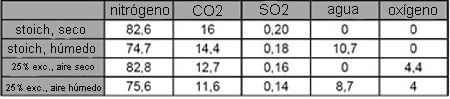
Efecto de dilución del contenido en humedad y del exceso de aire:
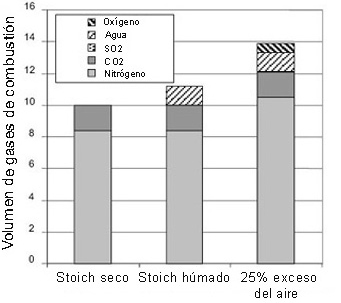
Diagrama de combustión:
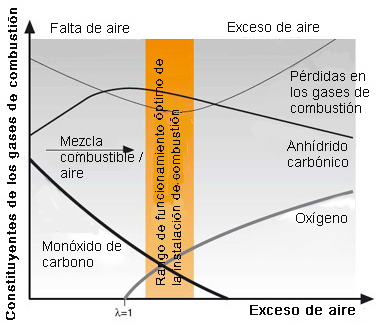

A partir de los hechos resumidos anteriormente, se puede concluir que las evaluaciones de las concentraciones solamente se pueden hacer, en general, en conjunción con valores de referencia. Solamente entonces tienen sentido las lecturas y se pueden comparar frente a otras mediciones y, sobre todo, ¡frente a los requisitos reglamentarios! En la práctica, se utiliza lo siguiente:
Con relación a una cierta dilución por el exceso de aire; el contenido de oxígeno es una medida de esto, y esta referencia se expresa por ejemplo como "valor de referencia 8% de oxígeno".
Un punto de referencia próximo al contenido de oxígeno que se produce cuando la instalación se hace funcionar en las condiciones estándar de la misma.
Con relación a una cierta dilución por el contenido de humedad del gas; la temperatura del gas es una medida de esto, y esta referencia se expresa por ejemplo como "referencia a gases de combustión secos" o "a punto de rocío de 4°C".
Con relación a las condiciones normales de un gas. Esto se refiere a la dependencia del volumen de un gas de los valores de presión y temperatura actuales.

Los gases de escape generados en los procesos de combustión se denominan gases de combustión. Su composición depende del tipo de combustible y de las condiciones de combustión, ej. el valor del coeficiente de exceso de aire. Muchos de los componentes de los gases de combustión son contaminantes del aire y por tanto deben eliminarse de los gases de combustión con procedimientos especiales de limpieza extremadamente lentos y costosos, antes de liberar el gas a la atmósfera conforme a la normativa legal. Los gases de combustión en su estado original se conocen como gases brutos y como gas limpio una vez que han pasado por las fases de limpieza. A continuación se explican los principales componentes de los gases de combustión.
Nitrógeno (N2):
Con el 79 % en volumen, el nitrógeno es el principal componente del aire. Este gas incoloro, inodoro e insípido se aporta mediante el aire de combustión pero no tiene un papel directo en la misma; pasa como medio inerte y medio para disipar el calor y se devuelve a la atmósfera. Sin embargo, el nitrógeno contribuye en parte, junto con el nitrógeno del combustible, a la formación de óxidos de nitrógeno peligrosos (ver a continuación).
Anhídrido carbónico (CO2):
El anhídrido carbónico es un gas incoloro e insípido, con un gusto ligeramente ácido, y se genera en todos los procesos de combustión y durante la respiración. Debido a su propiedad de filtrar el calor radiante, es una contribución importante al efecto invernadero. Su contenido en el aire ambiente es sólo del 0,03% y la concentración máxima permitida de anhídrido carbónico (CO2) en el puesto de trabajo es del 0,5%; concentraciones en el aire inhalado superiores al 15% producen la pérdida de conciencia en las personas.
Vapor de agua (humedad):
El hidrógeno contenido en el combustible se une con el oxígeno para formar agua (H2O). Dependiendo de la temperatura de los gases de combustión (FT), aparece luego conjuntamente con el agua del combustible y el aire de la combustión o como humedad de los gases de combustión (a FT alta) o como condensado (a FT baja).
Sustancias sólidas (polvo, hollín):
Las sustancias sólidas en los gases de combustión se originan a partir de los constituyentes incombustibles de los combustibles sólidos y líquidos. Estas incluyen, por ejemplo, óxidos de silicio, aluminio, calcio, etc., en el carbón y los sulfatos de diversas sustancias en el fueloil pesado. El efecto nocivo del polvo sobre las personas está producido particularmente por la deposición de sustancias tóxicas y cancerígenas en las partículas de polvo.
Oxígeno (O2):
El oxígeno no utilizado en el proceso de combustión, si hay exceso de aire, aparece como gas en los gases de combustión y es una medida de la eficiencia de la combustión. Se usa para determinar los parámetros de combustión y como variable de referencia.
Monóxido de carbono (CO):
El monóxido de carbono es un gas tóxico incoloro e inodoro. Se genera en gran medida como consecuencia de la combustión incompleta de combustibles fósiles (instalaciones de combustión), combustibles de motor (vehículos) y otros materiales que contienen carbono. El CO es, en general, inocuo para las personas porque rápidamente se une con el oxígeno del aire para formar CO2. En recintos cerrados, sin embargo, el CO es extremadamente peligroso, ya que las personas que respiran aire con una concentración de sólo 700 ppm morirán en pocas horas. La concentración máxima en el puesto de trabajo es 50 ppm
Óxidos de nitrógeno (NO y NO2, fórmula total NOx):
En los procesos de combustión, el nitrógeno del combustible y, a temperaturas elevadas, el del aire de combustión se une en cierta medida con el oxígeno del aire de combustión para formar óxido nítrico NO (NO combustible y NO térmico) en primera instancia, que luego se oxida cuando entra en contacto con el oxígeno en el conducto de los gases de combustión y posteriormente en la atmósfera, para formar el peligroso dióxido de nitrógeno (NO2). Ambos óxidos son tóxicos; el NO2 en particular es un peligroso veneno respiratorio y en combinación con la luz solar contribuye a la formación de ozono. Se utilizan tecnologías caras tales como el proceso SCR para limpiar los gases de combustión que contienen NOx. Medidas especiales relacionadas con la combustión, tales como el suministro de aire por etapas, se utilizan para reducir los óxidos nítricos en la etapa de combustión.
Anhídrido sulfuroso (SO2):
El anhídrido sulfuroso es un gas incoloro, tóxico con un olor picante. Se produce como resultado de la oxidación del mayor o menor volumen de azufre contenido en el combustible. La concentración máxima en el puesto de trabajo es 5 ppm. En combinación con agua o condensado, se forman ácido sulfuroso (H2SO3) y ácido sulfúrico (H2SO4), ambos de los cuales están relacionados con los diversos tipos diferentes de deterioro medioambiental a la vegetación y edificios. Las plantas de desulfuración de los gases de combustión (FGD) se usan para reducir los óxidos de azufre.
Sulfuro de hidrógeno (H2S):
El sulfuro de hidrógeno es un gas tóxico que huele mal incluso en concentraciones mínimas (aprox. 2,5 µm/m3). Es un componente que se encuentra naturalmente en el gas natural y el petróleo y por consiguiente está presente en refinerías e instalaciones de procesado de gas natural, pero también en tenerías, actividades agrícolas y, no de forma menos importante, tras la combustión incompleta en los convertidores catalíticos de vehículos. Se usan diversos métodos para eliminar el H2S de los gases de combustión, incluida la combustión para formar SO2, determinados procesos de absorción o, para niveles más importantes, la conversión en azufre elemental en una instalación Claus.
Hidrocarburos (HC o CxHy):
Los hidrocarburos son un amplio grupo de compuestos químicos formados exclusivamente por carbono e hidrógeno. Los HC son las sustancias más importantes en química orgánica; en la naturaleza se encuentran en el petróleo, gas natural o el carbón. Se pueden emitir HC cuando se fabrican productos hidrocarbonados (ej. en refinerías) así como durante su uso y eliminación (disolventes, plásticos, pinturas, combustibles, residuos, etc.). Las combustiones incompletas son una fuente particular de emisiones de HC. Estas también incluyen los incendios forestales y los cigarrillos, por ejemplo. Los HC también contribuyen al efecto invernadero. Ejemplos de HC incluyen metano (CH4), butano (C4H10) y benceno (C6H6), pero también componentes cancerígenos como el benzopireno. El potencial total de compuestos orgánicos volátiles en los gases de combustión normalmente se describe como HC total o CxHy total. Esta suma se determina generalmente en los gases de combustión.
Cianuro de hidrógeno (HCN):
El cianuro de hidrógeno (también conocido como ácido cianhídrico) es un líquido extremadamente venenoso con un punto de ebullición de 25,6°C; donde está presente, adopta la forma gaseosa en los gases de combustión. El HCN también puede encontrarse en instalaciones de incineración de residuos.
Amoníaco (NH3):
En los gases de combustión, el amoníaco juega un papel, conjuntamente con el proceso SCR, en la reducción de los óxidos de nitrógeno. Se añade a los gases de combustión en cantidades exactamente dosificadas en reactores de óxidos de nitrógeno y desencadena la conversión de los óxidos de nitrógeno en nitrógeno y agua. La parte no utilizada (pérdida de NH3) se reduce fuertemente mediante etapas de limpieza posteriores y está presente normalmente en los gases limpios a 2 mg/m3 o menos.
Haluros de hidrógeno:
Si se queman carbón y/o sustancias residuales, se producen los haluros de hidrógeno HCl y HF que, en combinación con la humedad, forman ácidos agresivos. Estas sustancias se lavan de los gases de combustión en gran medida, en las instalaciones limpiadoras de gases de combustión (lavadores).

Poder calorífico bruto, poder calorífico neto
El poder calorífico bruto (anteriormente denominado como potencia calorífica neta superior) es un valor característico del combustible y describe la energía liberada durante la combustión completa en relación con la cantidad de combustible aportada. El poder calorífico neto (anteriormente denominado como potencia calorífica neta inferior) es, por otra parte, la energía liberada menos el calor de evaporación del vapor de agua generado durante la combustión a 25°C, nuevamente en relación con la cantidad de combustible aportada. El poder calorífico neto es en general, inferior al poder de combustión.
Rendimiento de la combustión
El rendimiento es una variable que se determina mientras la instalación está funcionando de forma constante, a partir de los valores de potencia. El rendimiento (siempre es inferior al 100%) es la relación entre la energía total suministrada desde la cámara de combustión y la energía necesaria o utilizada para completar el proceso (calentamiento, fusión, sinterizado, etc.). El rendimiento incluye varias partes:
Calderas de condensación
Las calderas de condensación son calderas de calefacción que, además del calor de evaporación, también hacen uso del calor de condensación de los gases de combustión generados reenfriando el gas a la temperatura apropiada. En términos de poder calorífico neto, estas calderas pueden conseguir un rendimiento de combustión del 107%. Sin embargo, el condensado cargado de contaminantes así generado se debe eliminar de forma medioambientalmente segura.

En el modo de funcionamiento estacionario, la suma de todas las energías suministradas a la instalación debe ser igual a la suma de las energías emitidas por la instalación; véase la tabla que sigue.
Contribuciones para mantener el balance energético
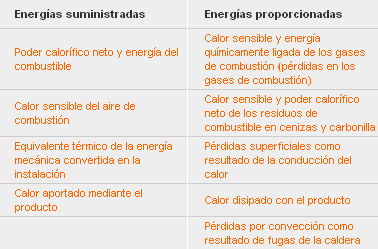
La parte principal de la pérdida son las pérdidas en los gases de combustión. Es función de la diferencia entre la temperatura de los gases de combustión y la temperatura del aire de combustión, de la concentración de O2 o CO2 en los gases de combustión y de factores específicos del combustible. En las calderas de condensación (véase anteriormente), estas pérdidas en los gases de combustión se reducen de dos formas, haciendo uso del calor de condensación y mediante la menor temperatura de los gases de combustión resultante. Las pérdidas en los gases de combustión se pueden calcular usando las siguientes fórmulas:
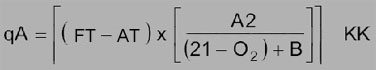
FT: Temperatura de los gases de combustión
AT: Temperatura del aire de combustión
A2, B: Factores específicos del combustible
21: Contenido de oxígeno del aire
O2: Concentración de O2 medida
KK: Variable que presenta la variable qA como valor negativo si no se alcanza el punto de rocío. Necesario para mediciones en calderas de condensación.
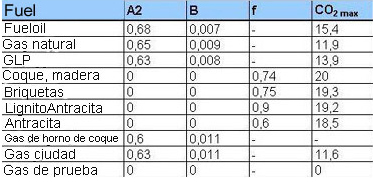
Para los combustibles sólidos, los factores A2 y B son iguales a cero. La fórmula se simplifica luego usando el factor f para obtener lo que se denomina como la fórmula de Siegert.
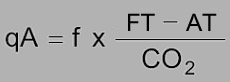
Los factores específicos del combustible usados en las fórmulas se indican a continuación.
Factores específicos del combustible:

Punto de rocío
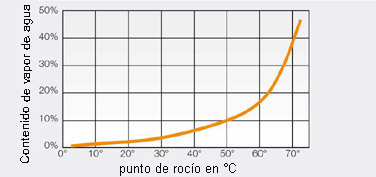
El punto de rocío o temperatura del punto de rocío de un gas, se entiende que significa la temperatura a la que la humedad contenida en el gas cambia del estado gaseoso al estado líquido; véase el diagrama que sigue. Esta transición se conoce como condensación, el líquido que se produce, condensado. La humedad aparece en estado líquido por debajo del punto de rocío y en estado gaseoso por encima del punto de rocío; un ejemplo de esto es la formación y evaporación de la niebla o el rocío, a medida que cambia la temperatura. El contenido de humedad determina la temperatura del punto de rocío. El aire con un 30% de contenido de humedad tiene un punto de rocío de alrededor de 70°C, mientras que el punto de rocío del aire seco con un contenido de humedad de sólo el 5% es aproximadamente 35°C.
Contenido de vapor de agua como función del punto de rocío
Nota sobre el contenido de vapor de agua
Si se mide con un instrumento sin preparación del gas, la temperatura del punto de rocío del gas corresponde en su mayor parte a la temperatura ambiente, es decir, 25°C, por ejemplo. Si estas mediciones se comparan luego con los valores medidos con preparación del gas, es decir, la temperatura del punto de rocío de 5 °C, por ejemplo, las diferencias resultantes en las lecturas debidas al diferente contenido de humedad ¡son aproximadamente del 3%!
Cifras de concentración
El término "concentración" describe la parte de una sustancia en el total de una mezcla sólida, gaseosa o liquida, ej., alcohol en la cerveza o el oxígeno en el aire. Se utilizan diversas mediciones para especificar una concentración, tales como:
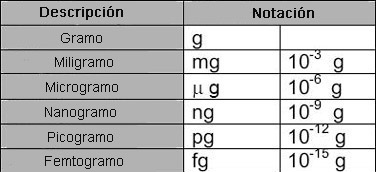
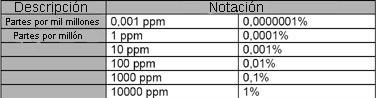
En la tecnología de emisiones e inmisiones, las unidades de concentración en peso y concentración de partículas se superponen. La unidad de masa usada en este caso es el gramo, o sus fracciones, mientras que el término ppm (partes por millón) es corriente para la concentración de partículas. Las fracciones de estas unidades se usan dependiendo de la concentración.
Por consiguiente, una cantidad de contaminantes se especifica así
Unidad de masa g con fracciones
Concentración de partículas ppm y % con fracciones
Nota sobre la concentración en peso
Debido a la dependencia general del volumen de un gas con su temperatura y su presión, también es necesario, para la certeza de una lectura cuando se usa la concentración en peso,
Después de esta clase de conversión, se indica luego el volumen en metros cúbicos normales (descritos como Nm3 o m3N).
Condiciones normales; volumen normal de un gas (VN)
El volumen de un gas depende de su temperatura y de la presión a la que esté.
Para comparar, se definió el volumen normal:
Un gas tiene su volumen normal si su temperatura y presión son idénticas a los valores definidos en las condiciones normales de 273 K (que corresponden a 0°C) y 1013 mbar (hPa).

Conversión a condiciones normales
Una lectura real (estado 1) se convierte a condiciones normales (estado 2) usando la fórmula:
c2 = c1 * ((T1 * p2) / (T2 * p1))
Nota sobre la fórmula anterior:
Las variables usadas en la fórmula significan lo siguiente:
Condición 1: Condición de medición T1:
Temperatura del gas a la medición (273 + temperatura real en °C)
p1: Presión de gas a la medición en hPa
c1: Concentración medida
Condición 2: Condición normal T2: Temperatura normal (= 273 K)
p2: Presión normal (= 1013 hPa)
c2: Concentración convertida a condiciones normales
Ejemplo: 200 mg/m3 a 35°C y 920 hPa producen 248,4 mg/Nm3 en condiciones normales después de la conversión
Concentración volumen/volumen (%v/v; ppm):
Una forma habitual de expresar la concentración de los gases es el valor volumen/volumen porcentual. Es decir:
Concentración porcentual de gas "X" (% vol/vol) = 100 * Volumen del gas contaminante "X" / volumen del gas total
Otra forma de expresar ese mismo valor de una forma más conveniente cuando ese valor de concentración es muy pequeño es pasarlo a ppm (abreviatura de partes por millón).
Conc. en partes por millón de gas "X" (ppm vol/vol) = 1000000 * Volumen del gas contaminante "X" / volumen del gas total
En otras palabras:
1% = 10000 ppm
Ejemplo:
En una chimenea a la salida de un proceso de combustión se tienen 15 cm3 de CO por cada 1000000 de cm3 de gas de combustión.
En tanto por uno: 15 cm3 /1000000 cm3 = 0,000015 de CO
En valor porcentual sería: 100 * 0,000015 de CO = 0,0015% de CO
En ppm (partes por millón), se observa que son "15 partes por millón" directamente en el enunciado. De la misma forma se obtendría multiplicando por un millón el valor en tanto por uno, es decir:
1000000 * 0,000015 de CO = 15 ppm de CO
Obsérvese que al expresar ambos volúmenes en la misma unidad, éstas se simplifican. El "%" y las "ppm" no son unidades físicas. Entonces la expresión de una concentración "volumen sobre volumen" es adimensional. La concentración masa/volumen, en cambio, sí tiene unidades.
Concentraciones volumen/volumen en base seca y en base húmeda:
Los analizadores de gases de combustión que poseen celdas electroquímicas para sensar los gases necesitan secar el gas de combustión antes de secarlo. Es decir, se remueve el vapor de agua del gas de combustión y ese vapor de agua retirado debe ser restado del volumen total de gas. Por lo tanto, en las concentraciones v/v vistas anteriormente, cuando se divide por "volumen total del gas", en realidad se divide por el "volumen total de gas seco". Y por lo tanto, la concentración está expresada en "base seca".
Si el método de medición no requiriese el secado del gas, se expresaría considerando el vapor de H2O en el volumen total. Es decir, en "base húmeda".
Ambas formas son correctas y siempre debe aclararse en qué base están expresadas las concentraciones. Los valores numéricos son distintos: al restarse el vapor de agua, el denominador es menor y por lo tanto la concentración en base seca es mayor que la misma concentración pero en base húmeda.
Reescribiendo las fórmulas anteriores con más detalle:
Concentración porcentual de gas "X" (% vol/vol) en base húmeda = 100 * Volumen del gas contaminante "X" / volumen del gas total húmedo
Cx (% vol/vol) base húmeda = 100 * Vol "X" / VGas-Húmedo (1)
Concentración porcentual de gas "X" (% vol/vol) en base seca= 100 * Volumen del gas contaminante "X" / volumen del gas total seco
Cx (% vol/vol) base seca = 100 * Vol "X" / VGas-Seco
Como el volumen del gas seco es el volumen total húmedo sustrayendo el vapor de agua
VGas-Seco= VGas-Húmedo - VH2O
y de forma análoga
VGas-Húmedo = VGas-Seco + VH2O
Considerando ésto, podemos pasar de base seca a base húmeda y viceversa si conocemos el valor del volumen o concentración de vapor de agua en el gas.
Cx (% vol/vol) base seca = Cx (% vol/vol base húmeda) / [ 100% - H2O% (v/v base húmeda)]
Cx (% vol/vol) base húmeda = Cx (% vol/vol) base seca * [ 100% - H2O% (v/v base húmeda)]
El valor de H2O% puede obtenerse analizando una muestra del gas por método gravimétrico o volumétrico (el equivalente en vapor de la cantidad de condensado obtenido a partir del secado de un volumen conocido de gas de combustión).
Secar un gas implica bajar la temperatura del mismo por debajo de su punto de rocío, para que condense todo el vapor de agua y pueda ser removido.
Ejemplo:
Se mide a la salida de un proceso el gas de combustión con un analizador portátil de gases de combustión que trabaja en base seca. El analizador muestra en pantalla un valor de O2% = 3,5%. Mediante otro método, se seca 1 m3 de ese gas de combustión (incluyendo el vapor de agua) y se determina que en ese metro cúbico había inicialmente 0,2 m3 de vapor de H2O.
Si se midiese con una sonda de O2 que trabaja en base húmeda (por ejemplo, una sonda de dióxido de circonio como la sonda lambda de los vehículos), ¿cuál sería el valor obtenido?
Respuesta:
O2 (% vol/vol) base húmeda = O2 (% vol/vol) base seca * [ 100% - H2O% (v/v base húmeda)]
por otro lado,
H2O% base húmeda = 100 * 0,2 m3 de H2O / 1 m3 de gas húmedo = 20% v/v base húmeda
Entonces
O2 (% vol/vol) base húmeda = 3,5% * [ 100% - 20%] = 2,8%
Un valor de 3,5% en base seca equivale a un 2,8% en base húmeda considerando que el contenido de vapor de agua del gas es del 20%.
Conversión de ppm a concentración masa/volumen:
Una especificación en [ppm] se puede convertir a la unidad de concentración en masa/volumen [mg/Nm3] (miligramos sobre metro cúbico normalizado) correspondiente, usando la densidad normal del gas en cuestión como factor para las fórmulas mostradas a continuación. La "dilución" de los gases de combustión por el aire (del exceso de aire y donde sea necesario por aportes de aire adicionales o por las posibles fugas en la instalación), de la cual la concentración de oxígeno es una medida, también se debe tener en cuenta. Por consiguiente, las lecturas deben ser convertidas, en general, a una determinada concentración de oxígeno (llamada "O2 de referencia"). Por esta razón, los valores de referencia de oxígeno correspondientes también se especifican siempre en los requisitos oficiales junto con los contaminantes.
Además, la concentración real de oxígeno medida, que es una medida de la dilución real, también es necesaria para la conversión (O2 en el denominador de la fórmula).
Fórmulas de conversión para los gases CO, NOx y SO2:

Nota sobre las fórmulas de conversión:
El factor numérico (1,25 etc.) usado en las fórmulas corresponde a la densidad normal del gas respectivo en Kg/m3. Se debe tener en cuenta lo siguiente:
Si la conversión se ha de realizar sin referencia al contenido de oxígeno, la fórmula se simplifica omitiendo el cociente, quedando para el CO:
CO[mg/m³] = CO[ppm] x 1,25 [Kg/m³]
Esto aplica igualmente a los demás gases.
Conversión de ppm a unidades relacionadas con la energía
Para representar la concentración de contaminantes en las dos unidades relacionadas con la energía, g/GJ y mg/kWh (1 kWh = 3,6 MJ), se requieren conversiones usando factores específicos del combustible (FF); consultar las fórmulas que siguen y la tabla para el factor FF.
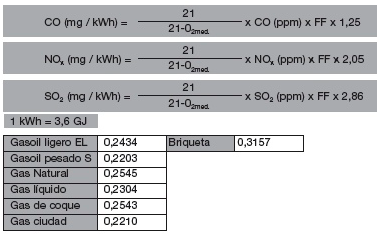
Fórmula para la conversión de ppm a g/GJ:
Teniendo en cuenta que 1kWh =3,6 MJ, entonces
1 g/GJ = 1000 mg / 1000MJ = 1000 mg/ (3,6x1000MJ) = 3,6 mg/kWh
1 g/GJ=3,6 mg/kWh, por lo tanto, multiplicamos cada una de las fórmulas anteriores por un factor de 3,6.

Los gases de combustión con un 8% humedad, por ejemplo, tienen un punto de rocío de alrededor de 40°C, lo que significa que se forma condensado por debajo de esta temperatura.
Esto tiene dos consecuencias importantes para la instalación en su conjunto así como para la tecnología de medición:
Consecuencia 1:
Si los gases de combustión contienen óxidos de azufre, estos se unen con el vapor de agua condensante a temperaturas inferiores a 40 °C (en las tuberías sin calentar, por ejemplo) para formar ácido sulfuroso (H2SO3) o ácido sulfúrico (H2SO4) que son, ambos, productos altamente corrosivos y pueden provocar considerables daños en aquellas partes de la instalación con las que entren en contacto. Por esta razón, la temperatura de los gases de combustión en la instalación se mantiene por encima del punto de rocío (es decir, superior a 40°C en el caso del ejemplo anterior) hasta que los gases de combustión llegan al lavador. Lo mismo aplica a aquellas partes de los instrumentos de medición a través de los cuales fluyen los gases de combustión y sobre todo a las piezas del dispositivo de muestreo, tales como sondas y mangueras. Por esta razón, se utilizan sondas y tuberías de medición del gas calentadas y su temperatura se mantiene por encima del punto de rocío del gas. ¡No hacerlo dará lugar al deterioro de los instrumentos de medición y a mediciones incorrectas!
Consecuencia 2:
Otra alternativa para evitar la formación de condensado es ofrecida por el método recientemente desarrollado y patentado por testo que consiste en una elevada velocidad de flujo del gas combinada con una superficie con un revestimiento especial en las tuberías de medición del gas. El resultado es que ya no es necesario calentar las tuberías, lo cual tiene mucha importancia en los dispositivos portátiles, a la vista de la reducción del consumo de potencia resultante. El vapor de agua está ausente de los gases de combustión gases enfriados en mayor o menor medida, dependiendo de la temperatura a la que se enfríe el gas, con el resultado de que los demás componentes del gas, tales como el CO, que no han cambiado cuantitativamente, forman una parte relativamente elevada de los gases de combustión; ¡las lecturas correspondientes son, pues, más altas que en los gases de combustión húmedos! Para lecturas comparables, el gas a medir respectivo debe, por consiguiente, tener las mismas temperaturas y por consiguiente el mismo contenido de humedad.
En consecuencia, los enfriadores del gas a medir (también podrían llamarse secadores del gas a medir) se usan en el análisis de gases antes del analizador; estos llevan el gas a una temperatura definida y por consiguiente un nivel definido de secado y lo mantienen allí.
Nota
Los dispositivos Testo utilizan lo que se conoce como un refrigerante Peltier para enfriar el gas a medir. Este funciona basándose en el principio de que las uniones entre dos tipos de metales diferentes se calientan o enfrían a medida que el gas fluye a su través, dependiendo del sentido del flujo.
Procesos para limpiar los gases de combustión:
Las emisiones de los contaminantes del aire contenidos en los gases de combustión se pueden reducir considerablemente tomando las medidas apropiadas o instalando las piezas necesarias en la instalación:
¡El análisis del gas para controlar y optimizar las mediciones, juega un papel vital en estos procesos
Las instalaciones para desempolvar flujos de gas (separador de polvos) trabajan basándose en diferentes principios:
Separación mediante la fuerza centrífuga o la fuerza de gravedad
En este caso, las partículas se desvían por la fuerza de la gravedad o por medio de fuerzas centrífugas en aquellas zonas del separador que están fuera de la corriente de gases de combustión. Ejemplos particularmente bien conocidos de este tipo de separación son los separadores basados en la fuerza centrífuga conocidos como ciclones, en los que las partículas adquieren un momento de inercia mediante una abertura de entrada de gas de diseño especial, que transporta las partículas a una cámara de separación. Desde allí entran en un recipiente colector del polvo.
Separación por medio de fuerzas eléctricas en precipitadores electrostáticos
Los precipitadores electrostáticos utilizan el efecto dinámico de un campo eléctrico sobre las partículas cargadas para separar el polvo.
Las partículas de polvo se cargan primero añadiendo iones negativos y luego, como consecuencia de esta carga, son conducidas a un electrodo colector en el campo eléctrico.
Allí se deposita el polvo como una capa; la capa se suelta (se limpia) golpeando el electrodo y el polvo se transporta a un depósito.
Los precipitadores electrostáticos se usan fundamentalmente para limpiar volúmenes muy grandes de gas en centrales eléctricas, acerías, fábricas metalúrgicas o cementeras, por ejemplo.
Separación por medio de adherencia a filtros fibrosos, por ejemplo
En esta forma, la separación de las partículas tiene lugar en el interior o en la superficie de determinados medios filtrantes (membranas, telas, fieltros) a través de los cuales fluye el gas.
Los más corrientes son los filtros de bolsas o mangas hechos de fibras.
Los filtros en profundidad incluyen, particularmente, los filtros de lecho, en los que tiene lugar la separación sobre la superficie del fieltro, a través del cual el gas fluye como una capa.
Separación mediante formación de gotas en torres de pulverización, por ejemplo
Aquí las partículas se unen con un líquido de lavado añadido al flujo de gas y se separan conjuntamente con este líquido.
El inconveniente de este proceso es que produce un líquido de lavado contaminado.
Info:
Con los precipitadores electrostáticos existe el riesgo básico de una explosión debido a la formación de una mezcla de gas explosiva dentro del campo eléctrico. Para una protección eficaz, se debe controlar el perfil de la concentración de CO antes del filtro.
Para reducir los óxidos de nitrógeno en los gases de combustión (o más exactamente para eliminar los óxidos de nitrógeno NO y NO2) se usan medidas primarias y/o, alternativamente, medidas secundarias.
Combustión en lecho fluido
En las calderas de lecho fluidizado el combustible de grano fino se transporta a la cámara de combustión encima de un suelo provisto de toberas. El aire de combustión fluye a través de las toberas desde abajo, haciendo que las partículas del combustible formen un lecho fluidizado. Las partículas sin quemar o totalmente quemadas se devuelven a la cámara de combustión desde la corriente de gases de combustión por medio de las medidas apropiadas, y se crea un lecho fluidizado circulante.
El proceso de lecho fluidizado ofrece significativas ventajas:
las partículas del combustible entran en un contacto muy íntimo con el oxígeno del aire de combustión y la combustión es, por consiguiente, casi completa. La temperatura de la combustión es alrededor de 900°C, lo que significa que hay una producción mínima de óxidos de nitrógeno térmicos; añadiendo cal al combustible, el combustible se puede desulfurizar ya durante la combustión.
Suministro de aire escalonado
Un suministro de aire escalonado es una medida primaria extraordinariamente eficaz, ya que reduce la formación del NO en el combustible y del NO térmico.
Esto reduce directamente el suministro de aire en el quemador (aire primario), el coeficiente de exceso de aire es por consiguiente <1, aumenta la formación de CO, el contenido de NOx permanece bajo y se reduce más por la formación de moléculas de N2 estables.
Luego se añade más aire de combustión (aire de incineración) sobre el quemador en una etapa posterior y garantiza que la combustión continúe.
Esto reduce significativamente el CO y se forma muy poco NO adicional, ya que el nitrógeno está ya presente como moléculas de N2 estables.
Quemadores de NOx bajo
De forma similar al suministro de aire escalonado en la cámara de combustión, estos quemadores funcionan con un suministro de aire distribuido en varios lugares del quemador y con una recirculación de aire interna.
Esto garantiza la combustión completa con formación reducida de óxidos de nitrógeno.
Proceso de desulfuración
De los muchos procesos para desulfurizar los gases de combustión, el lavado en húmedo con cal / piedra caliza (proceso secundario) se ha establecido como el principal favorito.
En una torre de lavado, los gases de combustión se pulverizan con una suspensión de lavado (piedra caliza finamente molida en agua), a consecuencia de lo cual la mayoría del anhídrido sulfuroso (SO2) se liga por medio de una reacción química.
El SO2 gaseoso se convierte inicialmente en una solución antes de combinarse como sulfato cálcico dihidratado (yeso).
Al menos parte de las grandes cantidades de yeso así generadas se reutilizan como material de construcción.
En la jerga técnica, la abreviatura FGD (desulfuración de gases de combustión) también se usa para instalaciones de esta clase.
Incineración térmica
En la incineración térmica, también conocida como limpieza térmica de los gases de combustión, los contaminantes del aire inflamables contenidos en los gases de combustión se queman con oxígeno en el aire a temperaturas entre 700°C y 900°C.
Esto produce CO y agua, pero, dependiendo de los contaminantes, también SO2, HCl y otros.
La incineración térmica es distinta de la combustión con llama, que trabaja a 1300°C, y de la combustión catalítica, que funciona a 250-500°C.
Las calderas de incineración térmica requieren, en general, una gran cantidad de energía (calderas suplementarias) y por consiguiente solamente se usan donde otras calderas no ofrecen el rendimiento suficiente o donde necesitan ser destruidos determinados constituyentes.
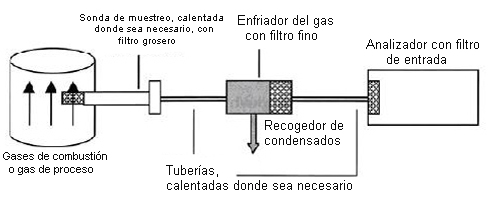
Muestreo extractivo
En la mayoría de los procesos de análisis de gases, el gas a medir se extrae del gas de proceso como una cantidad parcial que es lo más representativa posible (de aquí el nombre de proceso extractivo, a diferencia de los procesos in situ), se acondiciona y se introduce al analizador. El acondicionamiento (también denominado preparación de la muestra), consiste en limpiar el gas usando un filtro y, sobre todo, enfriando y por consiguiente secando el gas a un valor constante definido. Las ventajas de este método de medición son:
Los dispositivos para extraer y preparar el gas o están diseñados como unidades aparte o están combinados en una o más unidades compactas.
En términos sencillos, las funciones son:
Extracción y preparación de la muestra:

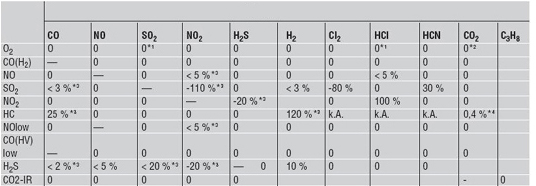
La sensibilidad cruzada de un sistema de detección es el resultado de no tener un rango infinito de resolución específica.
El sistema de detección es, por consiguiente, sensible con frecuencia no solo al componente que se está midiendo, y es de interés, sino, también en cierta medida, a otros componentes (componentes accesorios) en el gas a medir.
Los cambios en las concentraciones de estos componentes accesorios tienen un efecto sobre el valor medido del componente que realmente se mide, que se debe corregir en el dispositivo o retrospectivamente.
A este fin, también se deben medir los componentes accesorios. La sensibilidad cruzada se expresa en la forma del efecto (aumento o reducción) que tiene un componente accesorio del gas a medir sobre el valor del componente que se mide.
La magnitud de la sensibilidad cruzada depende del tipo de sistema de detección (¡por consiguiente es específico del dispositivo!) y de las concentraciones de los componentes accesorios.
Otras notas referentes a los efectos de los componentes accesorios:
Elevadas concentraciones de hidrocarburos no saturados pueden dar lugar a una deriva del cero y a una intensidad de respuesta reducida y, particularmente, en las células de medición de CO y NO.
Elevadas concentraciones de gases agresivos, tales como HCN, HCl o fluoruros, pueden atacar los trayectos del gas o la carcasa de la célula.
Contenido de humedad del gas:
El contenido de humedad del gas es una variable muy crítica en el análisis de gases por dos motivos:
Soluciones:
En general, impedir la formación de condensación en las piezas o en todo el equipo de medición usando un sistema de calentamiento en toda la instalación.
Sensibilidades cruzadas de BAL testo350:

Calibración
En la tecnología de medición la calibración se entiende que hace referencia al proceso de establecer y registrar el error de medición al que está sujeto el dispositivo terminado, preparado para funcionar. En el caso de la visualización de los instrumentos de medición, la discrepancia entre lo visualizado y el valor correcto del parámetro, o el valor que se supone que es correcto, se determina y registra usando factores o funciones. A diferencia del ajuste, el instrumento de medición no se modifica de ninguna forma durante la calibración.
La calibración es un elemento fundamental del aseguramiento de calidad en el control de las emisiones. Para la calibración se usan materiales de referencia cuya composición es conocida y con mucha exactitud. Para el análisis de gases, estos materiales de referencia son los gases de calibración (también conocidos como gases patrón).
Ajuste:
En la tecnología de medición ajuste se entiende que hace referencia al proceso de ajustar un instrumento de medición para que el error de medición sea el menor posible.
Este proceso implica una alteración del instrumento.
Calibración oficial:
Calibración Acreditada ENAC
Este tipo de calibraciones sólo puede llevarlas a cabo un laboratorio de de calibración Acreditado. Las acreditaciones a nivel nacional las realiza ENAC (Entidad Nacional de Acreditación). Otras entidades acreditadas en otros paises -DKD en Alemania, COFRAC en Francia, UKAS en Reino Unido, etc - y firmantes del acuerdo de reconocimiento mutuo (MLA) de certificados de calibración se reconocen mutuamente.
La diferencia principal entre un laboratorio que emite certificados trazables y certificados acreditados es que el laboratorio acreditados debe demostrar su capacidad técnica ante un auditor de la entidad de Acreditación.
Gas de prueba:
Un gas cuya composición se conoce con mucha precisión y se demuestra con certificados. Los gases de pruebas se utilizan para calibrar el analizador de gas.
Gas de prueba cero:
Gas de prueba usado para ajustar el punto cero de un analizador de gas. No debe contener el componente a medir (gas de proceso sin el componente a medir o nitrógeno, por ejemplo).
Gas accesorio:
Gas a medir sin el componente a medir.

Análisis de proceso
El análisis de proceso, a diferencia del análisis de laboratorio, hace referencia a los procesos de medición, normalmente continuos, que se utilizan para determinar las condiciones físicas o químicas o las concentraciones de componentes químicos en medios de proceso, in situ, en una instalación.
El análisis de proceso se usa con mayor frecuencia en las instalaciones industriales de productos químicos, petroquímicos, producción de energía, metales y minerales, materias primas alimenticias y alimentos de lujo, papel y pulpa, piedra y arcilla, sino, también, en la construcción de motores y en investigación y desarrollo, por ejemplo. En el caso de medios de proceso gaseosos (gases de combustión, gases de proceso, gases de escape, así como aire), se hace referencia al análisis de gases de proceso.
Por toda la instalación están distribuidos puntos de medición con el muestreo y los instrumentos de medición (analizadores de gases) en continuo (en la caldera, chimenea, horno de cemento, antes del precipitador electrostático, en una torre de destilación, etc.) en condiciones operativas extremadamente duras, en algunos casos. A la vista de esto, las diferencias con el análisis de laboratorio, donde se toman muestras discretas de un proceso y se examinan en un laboratorio en condiciones de laboratorio controladas y estables quedan claras.
El resultado de las mediciones se usa:
Analizadores:
El elemento central de cualquier analizador son sensores o sistemas de sensores específicos de la sustancia. Su funcionamiento está basado en principios físicos o químicos tales como la absorción, adsorción, transmisión, ionización, oxidación catalítica o propiedades paramagnéticas o electroquímicas. Los sensores reaccionan a un cambio en el parámetro con un cambio correspondiente en su propiedad (ej., aumento de la absorción de la luz o reducción de la conductividad), a partir de lo cual se puede obtener una señal de medición.
Por lo que respecta al diseño, se pueden clasificar en:
Gracias a los últimos avances se dispone de dispositivos que combinan movilidad y medición estacionaria a largo plazo.
Un ejemplo de esto es el analizador testo 360, que es fácilmente transportable aunque adecuado y está aprobado para mediciones a largo plazo durante varias semanas.

Sensores, formalmente, hace referencia a todos los tipos de dispositivos que proporcionan información acerca de una variable física o química.
Un sensor está compuesto por el sensor de medida real (también llamado el elemento sensor) y un transmisor. El sensor de medición debe tener una propiedad, ej., la conductividad, que también varíe con la variación de la variable a medir, tal como una temperatura. Esta "reacción" del sensor de medición se convierte luego en una señal de medición eléctrica por el transmisor (normalmente un amplificador).
Los principales grupos de sensores son:
El término sensor se usa con frecuencia de forma coloquial en la tecnología de análisis, solamente para aquellos sensores de medición que tienen unas dimensiones especialmente pequeñas, mientras que los sensores grandes se describen como un "analizador". Algunos de los sensores que se usan con frecuencia para determinar componentes de los gases se muestran en la tabla que sigue.
Sensores usados frecuentemente:

Dispositivos transportables:
Los requisitos de los analizadores transportables en la industria de proceso representan un reto particular para los fabricantes de equipos. En el duro ambiente de medición, la precisión necesaria y la fiabilidad de los valores de medición exigidos, junto con las dimensiones pequeñas y el poco peso del equipo, componen un perfil de requisitos que, hasta hace pocos años, no se podían cumplir. El desarrollo de los analizadores testo 350 y testo 360 ha marcado nuevos hitos que han recibido el aval con la emisión de las aprobaciones oficiales de estos dispositivos.
Los dispositivos testo 350 y 360 son dispositivos móviles que miden de forma extractiva y, debido a sus propiedades especiales (enfriador del gas a medir, calibración automática y otras), también se pueden usar en aplicaciones estacionarias durante un período de tiempo determinado. Por consiguiente abren nuevos campos de aplicación y ofrecen al usuario una solución muy rentable para diversas tareas. Idealmente, los sensores electroquímicos de gases, que son muy apropiados para dispositivos móviles debido a su poco peso, necesidades de espacio y consumo de energía, se usan como sensores. Sin embargo, su principio de funcionamiento requiere un considerable nivel de experiencia para garantizar la precisión, fiabilidad, duración y funcionalidad mediante el diseño del entorno correcto del sensor.
Principios de medición para verificar gases (selección):
Se utilizan diversos principios de medición para verificar los diferentes gases en mezclas de gas. La tabla que sigue aparece un resumen de los mismos junto con la referencia a los principios adoptados por Testo.
Componentes a medir y principios de medición apropiados para verificarlos:
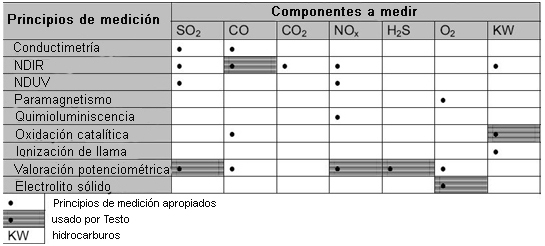
Los sensores electroquímicos adecuados para determinar el contenido de oxígeno y los constituyentes nocivos del gas tales como CO, SO2 o NOx, funcionan basándose en el principio de la valoración potenciométrica sensible a los iones.
Los sensores están rellenos con un electrolito acuoso, específico para la tarea, en el que están dispuestos dos o tres electrodos, igualmente combinados específicamente, entre los que hay un campo eléctrico. Los sensores están sellados del exterior mediante membranas permeables al gas.
El diseño específico y el funcionamiento de los sensores difieren según el componente del gas a medir, como se muestra usando dos ejemplos.
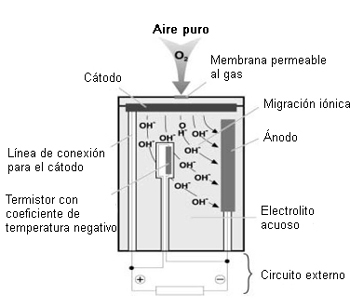
Ejemplo 1: Sensor de oxígeno (sensor de dos electrodos)
Los gases de combustión y las moléculas de oxígeno contenidas en ellos penetran a través de la membrana permeable al gas hasta el cátodo. Debido a su composición material, tiene lugar una reacción química en el cátodo con la formación de iones OH (los iones son partículas cargadas). Estos iones migran al ánodo a través del electrolito, creando un flujo de corriente proporcional a la concentración de O2. La caída de tensión desarrollada en una resistencia situada en el circuito sirve luego como señal de medición que se utiliza para el procesado electrónico posterior.
La resistencia incorporada con coeficiente de temperatura negativo (NTC), se usa para compensar los efectos de la temperatura, garantizando así que el sensor permanezca estable frente a los cambios de temperatura. La duración de un sensor de oxígeno de este tipo es de unos 3 años.
Ecuaciones de reacción del sensor de oxígeno:
En el cátodo: O2 + 2H2O + 4e- ------> 4OH-
En el ánodo: 2Pb + 4OH- ------> 2PbO + 2H2O + 4e-
Balance: 2Pb + O2 ------> 2PbO
Sensor de oxígeno (esquema)
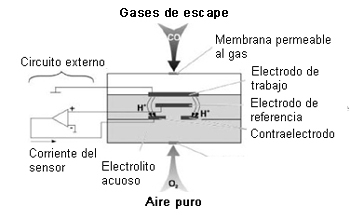
Ejemplo 2: Sensores para CO, SO2 y NOx (sensor de tres electrodos)
Para componentes del gas tales como CO, SO2 o NOx, se usan sensores con tres electrodos.
El funcionamiento se explica basándonos en un sensor de CO; cómo se aplica esto a los otros componentes se puede ver a partir de las ecuaciones de reacción.
Las moléculas de monóxido de carbono (CO) pasan, a través de la membrana permeable al gas, al electrodo de trabajo donde se forman iones H+ como consecuencia de una reacción química. Estos migran en el campo eléctrico al contraelectrodo, donde se genera un flujo de corriente en el circuito externo mediante otra reacción química desencadenada por el oxígeno (O2) del aire puro, también aportado. El tercer electrodo (electrodo de referencia) sirve para estabilizar la señal del sensor. La duración operativa de este tipo de sensor es de unos 2 años.
La duración de este tipo de sensor es alrededor de 2 años.
Ecuaciones de reacción para el CO
Ánodo: CO + H2O --------> CO2 + 2H+ + 2e-
Cátodo: 1/2 O2 + 2H+ + 2e- --------> H2O
Otras ecuaciones de reacción
SO2 + 2H2O ------> H2SO4 + 2H+ + 2e
NO + 2H2O ------> HNO3 + 3H+ + 3e-
NO2 + 2H+ + 2e- ----> NO + H2O
Sensor para CO y otros gases (esquema)
La radiación infrarroja es absorbida por gases tales como el CO, CO2, SO2 o NO, con una longitud de onda típica de cada componente (rango de longitud de onda de unas pocas µm). La atenuación de un determinado rango de radiación infrarroja a medida que un volumen de gas pasa a su través es, por consiguiente, una medida de las concentraciones del componente gaseoso en el gas a medir que ha pasado a su través. Hay dos métodos para incidir en solo un componente:
En el método dispersivo la radiación se descompone espectralmente mediante prismas o redes de difracción antes de que el volumen de gas pase a su través, después de lo cual solamente la radiación con la longitud de onda típica del componente que se está midiendo y es de interés, atraviesa el volumen del gas (cámara de medición). Este principio se usa en particular en los dispositivos de laboratorio.
En el método no dispersivo (método NDIR) se prescinde de la descomposición espectral descrita anteriormente, y una radiación de banda ancha, modulada con una rueda obturadora en todo el recorrido donde sea necesario, pasa a través de la cámara de medición.
Hay pues dos métodos para verificar la absorción:
>> O el propio componente a medir se usa en forma de un detector lleno con el mismo, de tal forma que el detector está lleno con el componente a medir y se mide la radiación residual aún presente después de que ha pasado a través de la cámara de medición, donde sea pertinente, comparando con la radiación sin atenuar. Las fluctuaciones de presión que se producen (debidas a las fluctuaciones en el calentamiento del volumen del gas como consecuencia de la absorción) se registran mediante un condensador de membrana o un sensor de microflujo y se convierten en una señal eléctrica.
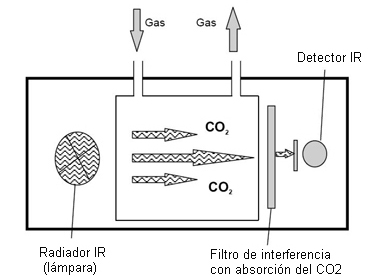
>> O, alternativamente, la radiación pasa a través de la sección de absorción y luego se contrae al rango de longitud de onda requerido para el CO2; por ejemplo, se verifica por medio de un filtro de interferencia usando un detector de radiación IR. A medida que aumenta la concentración del gas, se absorbe más radiación y la señal del detector se reduce en consonancia.
Sensor NDIR (diseño compacto) para medir CO2:

Los analizadores de conductor térmico (detectores de conductividad térmica estándar) utilizan la diferente conductividad térmica de los gases de medición y de referencia.
Un puente de hilo de medición a resistencias está rodeado en secciones por el gas a medir y por un gas de referencia con una conductividad térmica apropiada para la tarea de medición.
El diferente enfriamiento de los hilos de la resistencia produce un desequilibrio del puente, que se utiliza como el efecto a medir.
Oxidación catalítica
Este principio de medición está basado en el calor de evaporación de los constituyentes inflamables del gas a medir.
Estos se convierten catalíticamente en un cuerpo precalentado eléctricamente (alambre o pastilla) y a medida que se queman aumenta la temperatura del cuerpo, modificando su resistencia eléctrica.
El requisito para este principio de medición es un contenido de oxígeno adecuado en el gas a medir para la combustión.
El cambio de resistencia es una medida del contenido de (¡todos!) los constituyentes inflamables en el gas a medir.
En particular estos son hidrocarburos (abreviados a HC y también denominados como CxHy) pero, también, CO o H2.
Por consiguiente existen sensibilidades cruzadas entre estos componentes que deben ser tenidas en cuenta en la medición y en la evaluación de las lecturas.
Ejemplo
La lectura del hidrocarburo metano aumenta, por el CO también presente en el gas a medir, un 0,27 % en vol. por cada 1 % en vol. de CO. Para el hidrógeno, el incremento análogo es del 1,5 % en vol. por cada 1 % en vol. de H2.
Además, hay una sensibilidad cruzada al vapor de agua.
El módulo usado por Testo para medir hidrocarburos se basa en este principio.
Una corriente fluye a través de un hilo de platino, que calienta el hilo y el material catalítico aproximadamente a 500°C. Los componentes inflamables del gas a medir se queman en la superficie (en la medida que haya oxígeno suficiente para ello), elevando la temperatura del convertidor catalítico y del hilo de platino lo cual, a su vez, modifica la resistencia eléctrica del hilo y produce una señal de medición en un "circuito puente de Wheatstone".
Sensor basado en el principio de la oxidación catalítica
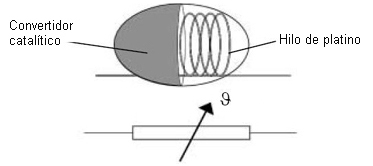
Se debe prestar una atención especial cuando se utilice el módulo Testo HC debido a sus sensibilidades cruzadas y al posible deterioro de su funcionamiento por sustancias presentes en el gas a medir tales como H2S, silicona o hidrocarburos sulfurados.
El manual de instrucciones del dispositivo proporciona la información pertinente.

Los compuestos orgánicos de carbono contenidos en el gas a medir se conducen al interior de una llama (normalmente hidrógeno / helio), se queman en esta llama y se ionizan en el proceso.
Los iones generados se miden como una corriente de iones que, en primera aproximación, es proporcional a los átomos de carbono orgánico involucrados en el proceso.
La diferente sensibilidad de este método por lo que respecta a los diferentes compuestos orgánicos se tiene en cuenta mediante factores de respuesta.
Sensor de electrolito sólido (1)
Un principio de medición especial, pero ampliamente utilizado, para medir oxígeno en condiciones operativas duras, utiliza un electrolito sólido de cerámica dopada con óxido de circonio, con n capas conductoras montadas en superficies enfrentadas como electrodos.
Como propiedad específica, este electrolito sódico contiene huecos de oxígeno en su red cristalina que facilitan la conductividad de los iones de oxígeno a temperaturas elevadas.
Las moléculas de oxígeno (O2) en el gas de proceso a medir se convierten en iones oxígeno cuando entran en contacto con el material del electrodo; si el electrolito está a una temperatura suficientemente elevada (>500°C), estos iones de oxígeno producen una corriente a través del electrolito.
Sensor de electrolito sólido (2)
Si la concentración de oxígeno es la misma en ambos lados, estos efectos aumentan, pero si las concentraciones son diferentes, se genera una corriente eléctrica aprovechable.
Si hay un gas de referencia con una concentración conocida de O2 en un lado, el contenido en O2 del gas a medir se puede determinar a partir de esta señal.
Los dispositivos que funcionan basándose en este principio se conocen como "sondas de óxido de circonio" o "sondas de oxígeno".
Generalmente se instalan directamente en los gases de combustión calientes (principio in situ) y por consiguiente miden el gas en sus condiciones originales, es decir, ¡con su humedad!
Sin embargo, como la humedad tiene un efecto de dilución sobre los otros componentes del gas, las lecturas de O2 de las sondas de esta clase son, en general, inferiores a las lecturas de O2 obtenidas en los mismos gases de combustión pero a temperaturas del gas inferiores, es decir, gases de combustión más secos, independientemente del método de medción utilizado.
Info:
Las lecturas de oxígeno de las sondas de circonio son, en general, inferiores a los valores obtenidos en el mismo gas mediante otros métodos, ¡pero ambos conjuntos de lecturas son válidos! La diferencia es atribuible a los diferentes grados de de dilución (temperaturas) del gas durante la medición; donde los valores se basen en las mismas temperaturas del gas (es decir, los mismos grados de dilución) ¡serán idénticas!
Testo utiliza este efecto en algunos de sus analizadores para medir la humedad en los gases de combustión usando el siguiente procedimiento:
El contenido de humedad original de los gases de combustión se puede calcular a partir de la diferencia entre las dos lecturas y la temperatura del enfriador.

Hay 3 métodos para medir gases de combustión
CTM 034
Este método de medida era publicar en 2005 de la Agencia de Protección del Medio Ambiente de Estados Unidos. CTM significa “Conditional Test Methods” porque la Agencia define métodos de ensayo que describen el uso de equipos de determinada tecnología para ciertas tareas de medición.
La Agencia de Protección del Medio Ambiente de Estados Unidos (comúnmente conocida como EPA por sus siglas en inglés, algunas veces USEPA) es una agencia del gobierno federal de Estados Unidos encargada de proteger la salud humana y proteger el medio ambiente: aire, agua y suelo.
Aplicabilidad
Este método es aplicable a la determinación de concentraciones de óxidos de nitrógeno (NO y NO2), monóxido de carbono (CO) y oxígeno (O2) en emisiones controladas y no controladas originadas en combustiones de combustibles como gas natural, propano, butano y petróleos. Este método está designado para proporcionar un alto grado de seguridad en el cumplimiento de normativas mediante la monitorización o comprobación periódicas. Este método no es adecuado para aquellos casos en los que se necesita un método de comprobación de referencia EPA. Además, debido a la sensibilidad cruzada inherente a los sensores electroquímicos, este método no se debería aplicar a otros contaminantes o fuentes de emisiones sin una investigación exhaustiva previa sobre posibles interferencias analíticas y una evaluación comparativa con otros métodos de comprobación EPA.
Principio
Se extrae una muestra de gas de la chimenea mediante un analizador de PdC portátil para la determinación de concentraciones de NO, NO2, CO y O2. Se deben conocer con exactitud las especificaciones técnicas y el manejo del analizador así como los procedimientos de comprobación para obtener datos fiables. Para cumplir con las especificaciones según los métodos de comprobación puede que se deban usar accesorios o se deba modificar la configuración del analizador (mangueras calentadas, termopares, anemómetros, etc.). No se pemite cambiar la configuración del analizador para que difiera de una verificación previa.
Análisis de los contaminantes presentes en muestras de emisiones gaseosas
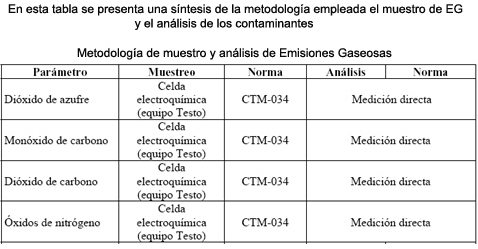

ASTM D-6522
Este método de medida era publicar en la “Annual Book of ASTM Standards” de la “American Section of International Association for Testing Materials”. ASTM o ASTM International es un organismo de normalización de los Estados Unidos de América.
ASTM International establece más de 14,000 normativas, documentos de especificaciones, métodos de comprobación, clasificaciones, procedimientos y directrices que describen las características de materiales, sistemas, productos y servicios. La ASTM está entre los mayores contribuyentes técnicos del ISO, y mantiene un sólido liderazgo en la definición de los materiales y métodos de prueba en casi todas las industrias, con un casi monopolio en las industrias petrolera y petroquímica.
Principios y aplicabilidad
ASTM D-6522
Método de comprobación estándar para la determinación de concentraciones de Óxidos de Nitrógeno, Monóxido de Carbono y Oxígeno en emisiones de motores de explosión de gas natural, turbinas de combustión, calderas y quemadores de procesos mediante analizadores portátiles.
Este método de comprobación abarca la determinación de las concentraciones de óxidos de nitrógeno (NO y NO2), monóxido de carbono (CO), y oxígeno (O2) en emisiones controladas y no controladas en motores de explosión de gas natural, turbinas de combustión, calderas y quemadores de procesos. Debido a la sensibilidad cruzada inherente a los sensores electroquímicos, este método de comprobación no es adecuado para otros contaminantes o fuentes de emisiones sin una investigación completa de posibles interferencias analíticas y una evaluación comparativa con métodos de comprobación EPA.
Los procedimientos y especificaciones de este método se desarrollaron durante los test en laboratorio y en campo originados por el Gas Research Institute (GRI).² Los test comparativos de emisiones solo se llevaron a cabo en fuentes de combustión con gas natural.
En el caso de los gases de combustión se aceptarán las mediciones según la norma ASTM D-6522, siempre que las instalaciones no se encuentren afectadas por el RD 653/2003 y el RD 430/2004.
Medidas relativas a la prevención de la contaminación atmosférica
Con respecto a la prevención de la contaminación atmosférica, los límites de emisión se han fijado de acuerdo con la legislación aplicable y los documentos de referencia europeos en relación con las mejores técnicas disponibles. Se fijan los límites de emisión siguientes.
Medidas relativas
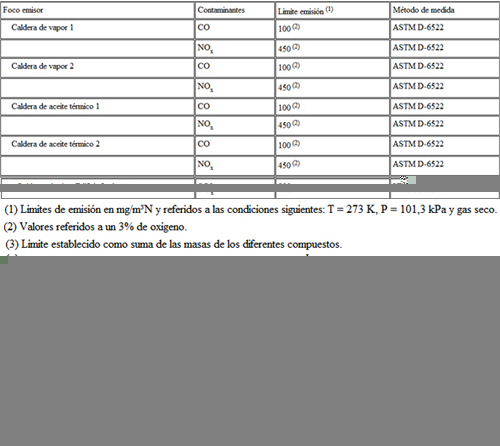

Métodos de referencia
Oxígeno - EN 14789
Se envía una muestra fresca y seca a un analizador paramagnético mediante un Analizador de PdC Horiba, método rápido y eficaz para medir niveles de oxígeno, y validado para muestreos de 30 minutos en el rango de 5 a 26%. Los resultados en O2 se ajustan al oxígeno de referencia y se muestran como mg/Nm3.
Monóxido de Carbono – EN 15058
Se envía una muestra fresca y seca a un analizador por medición directa de infrarrojos (NDIR) no dispersivo mediante un Analizador de PdC Horiba. Los resultados en CO se ajustan a la referencia y se muestran como mg/Nm3.
Este método se ha validado para concentraciones de CO en muestreos de 30 minutos en el rango de 0 mg/Nm3 a 400 mg/Nm3 para grandes plantas de combustión de 0 a 740 mg/Nm3 de incineración y residuos.
Óxidos de nitrógeno – EN 14792
Este método se realiza mediante quimiluminiscencia usando un Analizador de PdC Horiba. La columna de gas se enfría y se seca antes de que pase por el analizador. Los resultados en NOx se ajustan al oxígeno de referencia y se muestran como mg/Nm3.
Este método se usa tanto para rangos altos como bajos de concentraciones de NOx, calibrado mediante gases patrón UKAS trazables de referencia.
Dióxido de sulfuro – EN 14791
Se toma una muestra representativa mediante un sistema impinger mezclada con una solución diluida de peróxido de hidrógeno. Tras el muestreo, la solución impinger se analiza por cromatografía de iones para sulfato (SO4) y se ajusta al dióxido de sulfuro (SO2).
REAL DECRETO 430/2004,
De 12 de marzo, por el que se establecen nuevas normas sobre limitación de emisiones a la atmósfera de determinados agentes contaminantes procedentes de grandes instalaciones de combustión.
Esto Real Decreto se aplicará a las instalaciones de combustión cuya potencia térmica nominal sea igual o superior a 50 MW, cualquiera que sea el tipo de combustible que utilicen (sólido, líquido o gaseoso).
El tipo de medición es el siguiente:
Medición individual:
Antes de las mediciones individuales, se debe efectuar una medición inicial por Organismos de Control Autorizadas (OCA's) después de la construcción de una nueva instalación o de una modificación de importancia a una instalación existente. Esta medición inicial puede ser considerada como una aceptación de la instalación y se realiza antes de 3-12 meses desde la puesta en servicio. Las mediciones individuales se realizan posteriormente cada 3 años después de aquella. Las concentraciones de los gases nocivos sujetos a medición se determinan como valor medio a lo largo de un período de medición de media hora y se comprueba el cumplimiento de los valores límite.
Antes de la medición, el operador de la instalación debe ajustar la instalación de combustión a los valores óptimos de funcionamiento.
Medición continua:
Durante el funcionamiento diario de la instalación, cada media hora se calcula un "valor medio de media hora" a partir de los datos de medición registrados. Luego se calculan los "valores medios diarios" a partir de estos valores, se memorizan y se evalúan estadísticamente; no se deben superar los valores límite especificados para la instalación.
Analizadores para el control de las emisiones:
Los métodos de análisis usados para controlar las emisiones, actúan basándose en los mismos principios físicos o químicos usados en otros campos del análisis de gases. Sin embargo, los requisitos para los dispositivos son particularmente específicos aquí y los dispositivos deben demostrar el cumplimiento de las especificaciones en una prueba de cualificación.
El número de componentes contenidos en los gases de combustión requiere que los métodos y dispositivos sean suficientemente selectivos y que las sensibilidades cruzadas sean mínimas y de valor conocido. Los métodos de medición deben ser fiables y reproducibles y permitir la calibración. Además, se requiere una alta disponibilidad y una gran ausencia de tareas de mantenimiento.
Las tareas de medición también plantean requisitos particulares para el muestreo debido a la elevada temperatura de los gases de combustión, la elevada humedad y el contenido de polvo así como a los constituyentes agresivos de los gases de combustión. Además, cuando se toman muestras, se debe garantizar que las muestras sean representativas de la instalación, lo cual para las instalaciones con fuertes variaciones temporales y/o espaciales en los contaminantes, necesitará mediciones centrales o puntos de medición distribuidos individualmente, por ejemplo.
Prueba de cualificación para instrumentos de medición:
En determinadas aplicaciones solamente se pueden usar instrumentos de medición que hayan demostrado satisfactoriamente su cualificación para vigilar el control de la contaminación del aire.
La finalidad de este principio es garantizar la calidad y equivalencia de las mediciones y una práctica uniforme para supervisar las instalaciones. La prueba de cualificación se realiza según las recomendaciones prescritas (requisitos mínimos); se completa por medio de ensayos de laboratorio y una prueba de campo por unas pocas entidades de ensayo especialmente aprobadas. La demostración de una prueba de cualificación realizada satisfactoriamente se facilita mediante el correspondiente certificado o por medio de la publicación del resultado por el ministerio responsable en el que se denomina como el diario ministerial.
El analizador testo 360 ha pasado la prueba de cualificación para O2, CO, NO, NO2 y SO2 para las tareas de medición definidas en las normas CTM-034, ASTM D-6522 y los métodos de referencia EN 14789, EN 15058, EN 14792 y EN 14791.

La base para el control de las emisiones en los EE.UU. es la Clean Air Act (Ley de Limpieza del Aire) y los suplementos a la misma (Clean Air Act Ammendments (Enmiendas a la Ley de Limpieza del Aire), CAAA) publicadas en 1991. La CAAA es una ley federal. Con referencia a esta ley, la EPA (Agencia de Protección del Medio Ambiente) aprobó una reglamentación marco para reducir y controlar las emisiones. En particular, esto marcó un desplazamiento desde controlar fuentes de emisiones extremadamente grandes a controlar pequeñas fuentes (títulos 5 y 7).
Clasificación:
La CAAA divide las fuentes de emisiones en 7 secciones (títulos) con arreglo a su tamaño, de las que tres son especialmente importantes para el uso de los dispositivos testo:
Una fuente emisora se evalúa con arreglo a diversos criterios, ej., según la potencia calorífica o basándose en su potencial para emitir cantidades determinadas de contaminantes específicos, ej., 100 t NOx/año. Otras clasificaciones tratan de los valores límite permitidos para determinados tipos de instalaciones (partes) y las normas / recomendaciones para los instrumentos de medición (métodos).
Consecuencias:
El desplazamiento hacia instalaciones más pequeñas también tiene consecuencias para la tecnología de medición.
Los sistemas de medición continua en las instalaciones (CEMs - control de emisiones continuo) han sido y siguen siendo prescritos para controlar grandes emisarios; estos implican una inversión de varios cientos de miles de dólares con costes de mantenimiento anual de 30.000 dólares o más.
Estos costes son prohibitivos para los emisarios más pequeños, por lo que la EPA ya ha abierto el camino para otros equipos de medición más pequeños. ¡Esto también incluye el testo 360!
Reparto de la responsabilidad:
En los EE.UU., hay un reparto de la responsabilidad entre las autoridades federales y las autoridades de cada estado.
El título 4 está generalmente bajo la responsabilidad del gobierno federal, el título 7 bajo la responsabilidad de los estados; con el título 5 se concede a los estados responsabilidad si pueden proporcionar evidencia de actividades apropiadas para la puesta en marcha.
Para ejercer su responsabilidad, hay autoridades (Departamentos de Calidad Ambiental, DEQ) en cada estado que están facultados para introducir la norma establecida por la EPA o imponer una reglamentación más estricta.
La DEQ en California (Se llama el South Coast Air Quality Management District, SCAQMD) da empleo a 2400 personas y ha introducido varios reglamentos y métodos de medición específicos, tales como permitir el uso de dispositivos móviles para medir los NOx, por ejemplo.
Procedimiento:
Se definió un procedimiento especial para los emisarios menores de acuerdo con el título 7.
Las alrededor de 34.000 instalaciones afectadas han de ser evaluadas basándose en la reglamentación relativamente relajada (control de aseguramiento del cumplimiento, CAM) por las autoridades de cada estado a su discreción para establecer la necesidad de medidas.
¡Los métodos de medición ni están especificados ni están expresamente prohibidos aquí! Esto ha abierto un campo para nuevos procesos y dispositivos.
EPA:
La EPA no inspecciona ni certifica equipos.
Un ejemplo de ello es el método para medir determinados componentes del gas con sensores electroquímicos: en mayo de 2006 la EPA actualizó todos los métodos de ensayo instrumentales.
La EPA permite ahora todas las tecnologías de medición posibles para el O2, CO y NOx. La tecnología electroquímica no está restringida y se puede usar.
Además, el EPA CTM-030 es un método electroquímico que autoriza la medición de O2, CO y NOx.
Instrumentos Testo:
El testo 360 cumple con los métodos de ensayo 1 (para flujo de gas), 3 (para CO2 y O2), 6c (para SO2) y 7e en combinación con lo que se denomina como el método de ensayo condicional 022 (para NOx).
El testo 350 cumple los requisitos para los métodos de ensayo (TM030 y CTM 034). Además, la EPA publicó un informe de verificación:
(http://www.epa.gov/etv/verifications/vcenter1-26.html [1]).
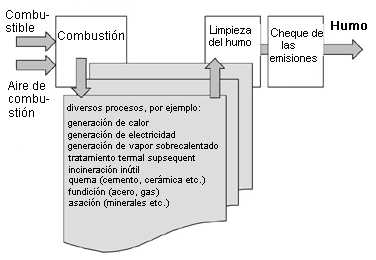
El análisis de gases (que es la tecnología de medición usada para determinar la composición de los gases) es una herramienta indispensable para garantizar la gestión económica y segura del proceso en virtualmente todos los campos de la industria.
Está enfocado a los procesos de combustión, aunque este es un término genérico que incluye un gran número de procesos diferentes. La Figura 6 muestra la secuencia de un proceso de combustión en secciones, que empieza (a la izquierda) con el aporte del combustible y del aire de combustión a una cámara de combustión, seguido por la combustión real y los diversos procesos ejecutados en su interior, pasando por la limpieza de los gases de combustión y la comprobación de las emisiones finales.
El análisis de gases proporciona información acerca de la composición de los gases de combustión y de los gases de escape en todas las fases de esta cadena de proceso. Es por consiguiente una herramienta indispensable para la operación económica y segura de la instalación en conformidad con la reglamentación oficial y, por consiguiente, también para la calidad y eficiencia de la producción.
Los analizadores de gases de Testo se usan ampliamente para analizar gases de combustión en la industria y en ninguna forma está reducido su empleo al campo específico del control de emisiones. Se puede hacer una distinción, con un cierto solapamiento, entre las siguientes aplicaciones:
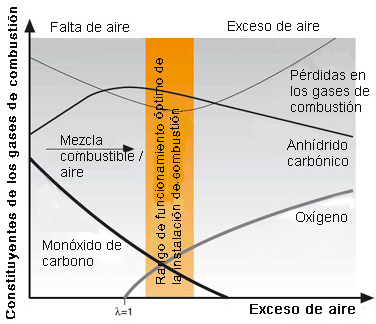
Factores particularmente esenciales en la optimización de la combustión son:
La relación óptima de combustible a cantidad de aire de combustión (coeficiente de exceso de aire λ) para una instalación dada y un combustible dado, se puede determinar a partir de las lecturas del análisis de gases usando lo que se llama el diagrama de combustión. Los perfiles de concentración de los componentes del gas CO, CO2 y O2 se muestran como función del coeficiente de exceso de aire.
La línea de combustión ideal con 0 exceso de aire (λ =1) está en el centro del gráfico, a su derecha el volumen de exceso de aire aumenta y a su izquierda aumenta el rango de insuficiencia de aire (¡falta de aire también significa insuficiencia de oxígeno!)
Los perfiles de concentración mostrados proporcionan la siguiente información:
Zona a la izquierda
Zona a la derecha
Conclusión
La combustión óptima se consigue si hay exceso de aire suficiente, y por consiguiente de oxígeno, para quemar todo el CO (rango de λ = desde 1,0 a aprox. 1,3) pero, al mismo tiempo hay un techo bajo de la cantidad de exceso de aire para que los menos gases de combustión calientes posibles, y por consiguiente de energía calorífica, se pierdan a la atmósfera como resultado de cantidades innecesariamente altas de exceso de aire.
El rango óptimo de λ para una instalación de combustión por lo que respecta a la energía (también depende de los datos específicos de la instalación) se puede determinar o midiendo el CO2 y el CO (¡el CO2 por sí solo es ambiguo ya que el perfil de su curva se extiende más allá de su límite máximo!) o midiendo solamente el O2. La última opción de medir el O2 se usa ampliamente ahora.
Dependiendo de la instalación y de su operario, los puntos de medición o de muestreo del gas pueden estar situados en varios puntos de la cámara de combustión.
Las correlaciones entre el coeficiente de exceso de aire, el exceso de aire y el contenido típico de oxígeno en los gases de combustión secos, mostrados en el gráfico se indican en cifras en la tabla que sigue para la combustión de antracita.
Correlación entre el exceso de aire y el contenido de oxígeno
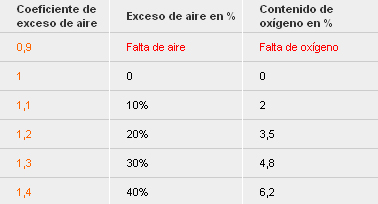
Además de reducir las emisiones, la finalidad principal de optimizar la combustión haciendo funcionar una instalación con la cantidad óptima, en general la mínima posible, de exceso de aire es reducir costes ahorrando combustible.
Instalación de combustión de proceso para procesos de combustión
A diferencia de las instalaciones de combustión convencionales (instalaciones de calderas de combustión), una instalación de combustión de proceso se caracteriza por el hecho de que hay contacto directo entre la combustión o los gases de combustión calientes y un producto a tratar térmicamente y que esto desencadena una serie de fases del proceso. La fabricación de clinker de cemento es un ejemplo que servirá para ilustrar otros procesos similares:
Análisis de gases:
El análisis de gases permite evaluar dichas fases del proceso por lo que respecta al exceso de aire, corrientes de aire exterior a calcular y las partes individuales de la instalación a equilibrar por separado. Esto es importante para el calcinador (medición de CO2 y O2), por ejemplo, ya que una calcinación insuficiente puede desencadenar perturbaciones significativas en el funcionamiento del horno. En procesos de esta clase, pueden pasar sustancias desde el producto que se procesa a los gases de combustión, incrementando las emisiones producidas por la instalación de combustión. En determinados casos, sin embargo, los contaminantes pueden, a la inversa, pasar desde el gas al producto que se procesa o a sustancias especialmente designadas (cenizas). Un ejemplo de esto es la industria del cemento o de la cal, en las que el azufre en el combustible se convierte en un constituyente del producto como óxido de azufre, en el proceso de combustión.
A la inversa, durante la fabricación del vidrio o de ladrillos, los óxidos de azufre se liberan del producto incrementando considerablemente la concentración de los gases de combustión. Hay una analogía con incremento de las emisiones de CO durante procesos que se realizan a contracorriente de la materia prima y los gases de combustión (ej., los hornos rotativos). En estos hornos, la cantidad de oxígeno en zonas alejadas del centro de la combustión puede ser insuficiente, dando lugar a una combustión incompleta con aumento de la concentración de CO.
Metales pesados pueden infiltrarse en el producto que se incinera (cemento, cal) y ser emitidos por el producto en los gases de combustión (industria metalúrgica, fabricación de vidrio). Las emisiones generadas por el proceso se pueden reducir significativamente mediante medidas relacionadas con el proceso tales como el diseño del horno, la gestión de la llama, la temperatura del producto que se incinera y del horno, el suministro de aire de combustión, etc. El análisis de gases proporciona la información necesaria para ello.
Calderas industriales:
El término caldera industrial se entiende que hace referencia a instalaciones de combustión usadas en la industria para producir calor y agua caliente y/u otros portadores de calor.
Esto también incluye las instalaciones de combustión para convertir sustancias en instalaciones de refinerías u hornos de coque, por ejemplo.
La producción de calor de las calderas industriales está en general, en el rango de los megavatios.
En el contexto de la reglamentación de emisiones dentro del ámbito de los Reales Decretos 833/1975, 653/2003 y 430/2004.
Las tareas del análisis de gases están orientadas en este caso a optimizar la combustión, comprobando la limpieza de los gases de combustión y controlando el cumplimiento con los valores límite.
Tratamiento superficial termoquímico:
Esta es una forma de tratamiento térmico en la cual la composición química de una pieza o de su superficie se modifica de una forma específica absorbiendo o expulsando determinados elementos de la atmósfera de gas ambiente.
Esto se utiliza sobre todo para endurecer el acero pero, también, para hornear vidriados y pinturas en la industria cerámica.
Estos procesos utilizan virtualmente sólo vidrio como medio de tratamiento (en casos raros también polvo) y difieren en naturaleza y concentración de los elementos introducidos por absorción (ej., nitrógeno en la nitruración, cromo en la cromización) y en las temperaturas de proceso (aproximadamente 400 - 1100 °C).
Los hornos continuos y por lotes entran en una amplia gama de diseños.
En todos los casos el análisis de gases requerido para garantizar el funcionamiento óptimo de la instalación (reducción de costes, seguridad) y para controlar la atmósfera de gas específica del proceso (calidad de producto, incluida la documentación de acuerdo con ISO 9000 ff.).
Los componentes más importantes a medir son O2, CO, CO2 y SO2.
Las aplicaciones del análisis de gases en procesos también pueden incluir mediciones diseñadas para proteger a las personas y a la instalación. Esto aplica a los gases tóxicos pero, sobre todo, a los inflamables y explosivos, particularmente al monóxido de carbono, CO. Los peligros de los incendios sin llama en los silos de polvo de carbón e instalaciones trituradoras de carbón pueden ser identificados por consiguiente en las fases iniciales controlando el CO y se puede evitar la formación de una mezcla de gas explosiva en los precipitadores electrostáticos. De forma similar, controlar las peligrosas concentraciones de metano u otros gases explosivos, particularmente en instalaciones químicas, puede ayudara prevenir situaciones peligrosas.
Límites de explosividad
Las mezclas de sustancias inflamables con aire u oxígeno son inflamables en determinadas concentraciones. Hay un límite de inflamación inferior y superior para cada mezcla. Estos valores dependen de la presión y de la temperatura: indican la parte del componente inflamable para ambos límites a una determinada temperatura y una determinada presión (generalmente 20°C y 1 bar) en % en volumen o en g/m3. El rango de inflamación o de explosión está entre estos dos límites, véase la tabla que sigue.
Límites de inflamación de gases inflamables
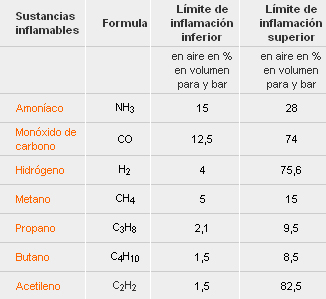
El principio de medición "oxidación catalítica" se usa para analizar mezclas de gas en componentes inflamables, aunque éste determina la suma de todos componentes inflamables. El rango de medición del dispositivo debe estar basado, por consiguiente, en el componente con el límite de explosividad inferior más bajo cuando se controla por el límite de explosividad inferior de una mezcla.
Análisis de gases para comprobar emisiones
La operación de instalaciones industriales de cualquier clase que sea (grandes centrales eléctricas, acerías, cementeras, vidrierías, industrias químicas y muchas otras), desde instalaciones municipales a pequeñas fábricas, están sujetas, en la mayoría de los países, a una estricta reglamentación por lo que respecta a las emisiones de gases de combustión a la atmósfera.
Se debe asegurar y verificar con regularidad, mediante las medidas pertinentes, que los componentes definidos como contaminantes no superen determinados valores límite en los gases de combustión. Cada país ha aprobado leyes y reglamentos en este campo, y de gran alcance en algunos casos; en España existen los Reales Decretos sobre emisiones, en Alemania existe la Ley Federal de Control de Inmisiones, mientras que en los EE.UU. existe la Ley de Limpieza del Aire. No existe una reglamentación estándar para toda Europa o toda Asia. Por consiguiente muchos países basan sus reglamentaciones nacionales.
El análisis de gases juega un papel fundamental en la puesta en marcha y el control de las medidas requeridas para limitar las emisiones..
Info:
Emisión: Las contaminaciones del aire, ruidos, vibraciones, calor, etc. que salen de una instalación (fuente)
Inmisión: Las contaminaciones del aire, ruidos, vibraciones, etc. que actúan sobre las personas, animales, instalaciones, terreno, edificios, etc.
Enlaces:
[1] http://www.epa.gov/etv/verifications/vcenter1-26.html